|
Lei n.ş 99/2017, de 25 de Agosto (versăo actualizada) O diploma ainda năo sofreu alteraçőes |
|
| SUMÁRIO Procede ŕ segunda alteraçăo ŕ Lei n.ş 12/2009, de 26 de março, que estabelece o regime jurídico da qualidade e segurança relativa ŕ dádiva, colheita e análise, processamento, preservaçăo, armazenamento, distribuiçăo e aplicaçăo de tecidos e células de origem humana, e transpőe as Diretivas 2015/565/UE e 2015/566/UE, da Comissăo, de 8 de abril de 2015 _____________________ |
|
Artigo 11.ş
Contratos |
1 - Os bancos de tecidos e células importadores devem celebrar contratos escritos com os fornecedores de países terceiros, sempre que uma atividade de dádiva, colheita, análise, processamento, preservaçăo, armazenamento ou exportaçăo para a Uniăo Europeia de tecidos e células, destinados a ser importados, seja realizada fora da Uniăo Europeia.
2 - O contrato deve especificar os requisitos de qualidade e segurança a respeitar, para garantir a qualidade e segurança dos tecidos e células a importar, de acordo com as normas estabelecidas na Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo, e incluir, no mínimo, as disposiçőes referidas no anexo VI da presente lei, da qual faz parte integrante.
3 - O contrato deve garantir ŕ DGS, o direito de inspecionar, em articulaçăo com a Inspeçăo-Geral das Atividades em Saúde (IGAS), as atividades, incluindo as instalaçőes, de qualquer fornecedor de um país terceiro, durante o seu período de vigęncia e por um período de dois anos após o seu termo.
4 - O banco de tecidos e células importador deve fornecer cópias dos contratos celebrados com os fornecedores de países terceiros ao IPST, I. P., no âmbito do seu pedido de autorizaçăo.
5 - O disposto no presente artigo năo se aplica ŕs importaçőes pontuais referidas no n.ş 2 do artigo 9.ş |
| |
|
|
|
|
Artigo 12.ş
Inspeçőes e outras medidas de controlo |
1 - A DGS garante, em articulaçăo com a IGAS, a realizaçăo de inspeçőes e outras medidas de controlo adequadas aos bancos de tecidos e células importadores e, se for caso disso, aos seus fornecedores de países terceiros, garantindo ainda que aqueles bancos realizam controlos adequados, para garantir a equivalęncia das normas de qualidade e segurança dos tecidos e células a importar, de acordo com as normas estabelecidas na Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo.
2 - O intervalo das inspeçőes năo deve exceder dois anos, devendo os profissionais envolvidos nas inspeçőes:
a) Estar mandatados para inspecionar o banco de tecidos e células importador e, se for caso disso, as atividades de qualquer fornecedor de um país terceiro;
b) Avaliar e verificar os procedimentos e atividades do banco de tecidos e células importador e as instalaçőes dos fornecedores de países terceiros que sejam relevantes para assegurar a qualidade e segurança dos tecidos e células a importar, de acordo com as normas estabelecidas na Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo;
c) Examinar quaisquer documentos ou outros registos que sejam relevantes para essa avaliaçăo e verificaçăo.
3 - A DGS deve, mediante pedido devidamente justificado de outro Estado membro ou da Comissăo Europeia, facultar informaçőes sobre os resultados das inspeçőes e outras medidas de controlo relacionadas com o banco de tecidos e células importador e os fornecedores de países terceiros.
4 - Mediante pedido devidamente justificado de outro Estado membro onde os tecidos e células importados sejam subsequentemente distribuídos, a DGS pode ainda realizar inspeçőes ou outras medidas de controlo do banco de tecidos e células importador e das atividades de qualquer fornecedor de um país terceiro, devendo decidir quais as medidas adequadas a tomar, após consultar o Estado membro que solicitou essas inspeçőes ou medidas.
5 - Na sequęncia do pedido referido no número anterior, a DGS pode determinar, em acordo com a autoridade competente do Estado membro que apresentou o pedido, a participaçăo deste último nas inspeçőes, devendo uma eventual recusa ser devidamente fundamentada e comunicada ao Estado membro requerente. |
| |
|
|
|
|
Artigo 13.ş
Registos das atividades dos bancos de tecidos e células importadores |
1 - Os bancos de tecidos e células importadores devem conservar um registo das suas atividades, incluindo as importaçőes pontuais efetuadas, mencionando os tipos e quantidades de tecidos e células importados, bem como a sua origem e seu destino.
2 - As atividades referidas no número anterior devem ser incluídas no relatório previsto no n.ş 4 do artigo 10.ş da Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo.
3 - O IPST, I. P., deve incluir os bancos de tecidos e células importadores no registo público previsto no n.ş 5 do artigo 10.ş da Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo.
4 - A informaçăo relativa ŕ autorizaçăo dos bancos de tecidos e células importadores deve também ser disponibilizada através do Compęndio dos Bancos de Tecidos e Células da Uniăo Europeia, referido no artigo 8.ş-D da Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo. |
| |
|
|
|
|
CAPÍTULO IV
Disposiçőes finais e transitórias
| Artigo 14.ş
Norma transitória |
1 - Os tecidos e células que se encontrem armazenados ŕ data da entrada em vigor da presente lei estăo isentos das obrigaçőes relativas ao Código Único Europeu previstas na Lei n.ş 12/2009, de 26 de março, com a redaçăo que lhe foi dada pela presente lei, desde que sejam colocados em circulaçăo no prazo máximo de cinco anos a contar da referida data, e desde que seja assegurada a plena rastreabilidade através de meios alternativos.
2 - No caso de tecidos e células que permaneçam armazenados e que sejam colocados em circulaçăo após o período referido no número anterior, em relaçăo aos quais năo seja possível a aplicaçăo do Código Único Europeu, os bancos de tecidos e células devem utilizar os procedimentos aplicáveis aos produtos com rótulos de pequena dimensăo, de acordo com o previsto no n.ş 3 do artigo 8.ş-C da Lei n.ş 12/2009, de 26 de março, com a redaçăo que lhe foi dada pela presente lei. |
| |
|
|
|
|
Artigo 15.ş
Norma revogatória |
|
Artigo 16.ş
Entrada em vigor |
A presente lei entra em vigor 30 dias após a sua publicaçăo.
Aprovada em 7 de julho de 2017.
O Presidente da Assembleia da República, Eduardo Ferro Rodrigues.
Promulgada em 3 de agosto de 2017.
Publique-se.
O Presidente da República, Marcelo Rebelo de Sousa.
Referendada em 7 de agosto de 2017.
O Primeiro-Ministro, António Luís Santos da Costa. |
| |
|
|
|
|
(a que se refere o artigo 4.ş)
Alteraçăo aos anexos I, III, V, IX, X e XI da Lei n.ş 12/2009, de 26 de março
«ANEXO I
[...]
a) ...
b) ...
c) ...
d) ...
e) ...
f) 'Código Único Europeu' ou 'SEC' (Single European Code), o identificador único aplicado aos tecidos e células distribuídos na Uniăo, composto por uma sequęncia de identificaçăo da dádiva e uma sequęncia de identificaçăo do produto, previsto no anexo XI da presente lei;
g) 'Código do banco de tecidos e células da UE', o identificador único dos bancos de tecidos e células autorizados, constituído por um código do país de acordo com a ISO 3166-1 e o número do banco de tecidos e células registado no compęndio de bancos de tecidos e células da UE, previsto no anexo XI da presente lei;
h) 'Código do produto', o identificador do tipo específico de tecidos e células, constituído pelo identificador do sistema de codificaçăo do produto, indicando o sistema de codificaçăo utilizado pelo banco de tecidos e células ('E' para EUTC, 'A' para 'ISBT128', 'B' para 'Eurocode'), e o número de produto dos tecidos e células previsto no respetivo sistema de codificaçăo para o tipo de produto, previsto no anexo XI da presente lei;
i) 'Colocar em circulaçăo', distribuir para aplicaçăo em seres humanos ou transferęncia para outro operador, nomeadamente para processamento adicional, com ou sem retorno;
j) [Anterior alínea f).]
k) 'Compęndio dos Bancos de Tecidos e Células da UE', o registo de todos os bancos de tecidos e células autorizados pela(s) autoridade(s) competente(s) dos Estados membros e que contém a informaçăo sobre esses serviços, prevista no anexo XII da presente lei;
l) 'Compęndio dos Produtos de Tecidos e Células da UE', o registo de todos os tipos de tecidos e células que circulam na Uniăo Europeia e dos respetivos códigos dos produtos, no âmbito dos tręs sistemas permitidos de codificaçăo (EUTC, ISBT128 e Eurocode);
m) [Anterior alínea g).]
n) [Anterior alínea h).]
o) [Anterior alínea i).]
p) [Anterior alínea j).]
q) 'Data de validade', a data até ŕ qual os tecidos e células podem ser aplicados, prevista no anexo XI da presente lei;
r) [Anterior alínea l).]
s) 'EUTC', o sistema de codificaçăo de produtos para os tecidos e células desenvolvido pela Uniăo Europeia, composto por um registo de todos os tipos de tecidos e células que circulam na Uniăo e os códigos de produto correspondentes;
t) [Anterior alínea m).]
u) [Anterior alínea n).]
v) [Anterior alínea o).]
w) [Anterior alínea p).]
x) 'No mesmo centro', o facto de todas as etapas, desde a colheita até ŕ aplicaçăo em seres humanos, serem realizadas num centro de cuidados de saúde que inclua, pelo menos, e no mesmo local, um banco de tecidos e células autorizado e um serviço responsável pela aplicaçăo em seres humanos, sob a responsabilidade da mesma pessoa e mesmos sistemas de gestăo da qualidade e rastreabilidade;
y) 'Número de fracionamento', o número que distingue e identifica de forma única os tecidos e células com o mesmo número único de dádiva e o mesmo código de produto e provenientes do mesmo banco de tecidos e células, como especificado no anexo XI da presente lei;
z) 'Número único da dádiva', o número único atribuído a cada dádiva de tecidos e células, em conformidade com o sistema em vigor em cada Estado membro para a atribuiçăo dos referidos números, como especificado no anexo XI da presente lei;
aa) [Anterior alínea q).]
bb) 'Plataforma de Codificaçăo da UE', a plataforma informática gerida pela Comissăo, que contém os compęndios dos bancos de tecidos e células e dos produtos de tecidos e células da Uniăo Europeia;
cc) 'Pooling', o contacto físico, ou mistura num único recipiente, de tecidos ou células provenientes de mais do que uma colheita do mesmo dador, ou de dois ou mais dadores;
dd) [Anterior alínea r).]
ee) [Anterior alínea s).]
ff) [Anterior alínea t).]
gg) [Anterior alínea u);
hh) [Anterior alínea v).]
ii) [Anterior alínea x).]
jj) [Anterior alínea z).]
kk) [Anterior alínea aa).]
ll) 'Sequęncia de identificaçăo da dádiva', a primeira parte do Código Único Europeu, constituída pelo código do banco de tecidos e células da Uniăo Europeia e o número único da dádiva;
mm) 'Sequęncia de identificaçăo do produto', a segunda parte do Código Único Europeu, constituída pelo código do produto, o número de fracionamento e a data de validade;
nn) [Anterior alínea ab).]
oo) [Anterior alínea ac).]
pp) [Anterior alínea ad).]
qq) [Anterior alínea ae).]
rr) [Anterior alínea af).]
ss) [Anterior alínea ag).
ANEXO III
[...]
...
A - [...]
...
B - [...]
...
1 - ...
2 - ...
3 - ...
4 - ...
5 - ...
6 - ...
7 - ...
8 - ...
C - [...]
...
1 - ...
2 - ...
3 - ...
4 - ...
5 - ...
6 - ...
7 - ...
D - [...]
...
1 - ...
2 - ...
3 - ...
4 - ...
5 - ...
6 - ...
7 - ...
8 - ...
E - [...]
1 - ...
a) ...
b) ...
c) ...
d) ...
e) ...
f) ...
g) O Código Único Europeu aplicável aos tecidos e células distribuídos para aplicaçăo em seres humanos ou a sequęncia de identificaçăo da dádiva aplicável aos tecidos e células colocados em circulaçăo para fins relacionados com processos de preparaçăo prévios ŕ sua distribuiçăo;
h) Caso năo seja possível incluir no rótulo do contentor primário as informaçőes mencionadas nas alíneas d), e) e g), estas devem ser fornecidas em documentaçăo própria, que acompanhará o referido contentor.
2 - ...
a) ...
b) ...
c) ...
d) ...
e) ...
f) ...
g) ...
h) ...
i) ...
j) No caso de tecidos e células importados, o país de colheita e o país de exportaçăo caso sejam diferentes.
F - [...]
...
ANEXO V
[...]
...
1 - ...
1.1 - ...
1.1.1 - ...
1.1.2 - ...
1.1.3 - ...
1.1.4 - ...
1.1.5 - ...
1.1.6 - ...
1.1.7 - ...
1.1.8 - ...
1.1.9 - ...
1.1.10 - ...
1.1.11 - Ingestăo de substâncias ou exposiçăo a substâncias, tais como organofosforados, cianeto, chumbo, mercúrio ou ouro, que possam ser transmitidas aos recetores em doses suscetíveis de pôr em risco a sua saúde;
1.1.12 - ...
1.1.13 - ...
1.2 - ...
2 - ...
ANEXO IX
[...]

ANEXO X
Dados mínimos a conservar em conformidade com o artigo 8.ş
A - ...
...
...
Identificaçăo do organismo de colheita (incluindo os contactos) ou do banco de tecidos e células;
...
...
...
...
...
...
...
...
...
Data de validade (se aplicável);
...
...
Código Único Europeu (se aplicável);
...
...
...
B - ...
a) ...
b) ...
c) ...
d) ...
e) ...
f) ...
g) Código Único Europeu (se aplicável).
ANEXO XI
Informaçăo contida no Código Único Europeu
a) Sequęncia de identificaçăo da dádiva:
i) Código do banco de tecidos e células;
ii) Número único da dádiva;
b) Sequęncia de identificaçăo do produto:
i) Código do produto;
ii) Número do fracionamento;
iii) Data de validade.
Estrutura do Código Único Europeu
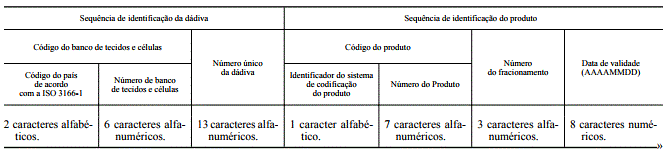 |
| |
|
|
|
|
(a que se refere o artigo 5.ş)
Aditamento do anexo XII ŕ Lei n.ş 12/2009, de 26 de março
«ANEXO XII
Dados a registar no Compęndio dos Bancos de Tecidos e Células da UE
A - Informaçăo sobre o banco de tecidos e células:
1 - Nome do banco de tecidos e células;
2 - Código nacional ou internacional do banco de tecidos e células;
3 - Nome da instituiçăo em que banco de tecidos e células está localizado (se aplicável);
4 - Endereço do banco de tecidos e células;
5 - Contactos publicáveis: correio eletrónico funcional, telefone e fax;
B - Informaçăo sobre a autorizaçăo do banco de tecidos e células:
1 - Nome da(s) autoridade(s) competente(s) de autorizaçăo;
2 - Nome da(s) autoridade(s) nacional(ais) competente(s) responsável(eis) pela manutençăo do compęndio dos bancos de tecidos e células da UE;
3 - Nome do titular da autorizaçăo (se aplicável);
4 - Tecidos e células para os quais foi concedida autorizaçăo;
5 - Atividades efetivamente realizadas para as quais foi concedida autorizaçăo;
6 - Estado da autorizaçăo (concedida, suspensa, revogada, no todo ou em parte, cessaçăo voluntária da atividade);
7 - Detalhes sobre eventuais condiçőes e isençőes aditadas ŕ autorizaçăo (se aplicável).» |
| |
|
|
|
|
(a que se refere o n.ş 2 do artigo 8.ş)
Certificado de autorizaçăo de um banco de tecidos e células importador
 |
| |
|
|
|
|
(a que se refere o n.ş 1 do artigo 9.ş)
Requisitos mínimos relativos ŕ informaçăo e documentaçăo a apresentar pelos bancos de tecidos e células para efeitos de autorizaçăo da atividade de importaçăo
Ao requerer a autorizaçăo, os bancos de tecidos e células devem fornecer as informaçőes e documentaçăo mais atualizadas a seguir indicadas:
1 - Informaçőes gerais sobre o banco de tecidos e células que pretende realizar atividade de importaçăo:
a) Nome do banco de tecidos e células, endereço para visitantes e, se diferente, endereço postal;
b) Estatuto do banco de tecidos e células:
i) Deve ser indicado se este constitui o primeiro pedido de autorizaçăo enquanto banco de tecidos e células importador, ou, se for caso disso, se se trata de um pedido de renovaçăo;
ii) Nos casos em que já se encontre autorizado como banco de tecidos e células, deve ser fornecido o código do compęndio de Serviço Manipulador de Tecido;
c) Nome da unidade requerente, se diferente do nome do banco de tecidos e células, endereço para visitantes e, se diferente, endereço postal;
d) Nome do local de receçăo das importaçőes, se diferente do nome do banco de tecidos e células e da unidade requerente, endereço para visitantes e, se diferente, endereço postal.
2 - Dados da pessoa de contacto do requerimento:
a) Nome da pessoa de contacto do requerimento, número de telefone e endereço de correio eletrónico, bem como, se diferente, nome da pessoa responsável, respetivo número de telefone e endereço de correio eletrónico;
b) Endereço da Internet do banco de tecidos e células, se disponível.
3 - Informaçăo detalhada sobre os tecidos e células a importar:
a) Lista dos tipos dos tecidos e células a importar, incluindo as importaçőes pontuais de tipos específicos de tecidos ou células;
b) Nome do produto, em conformidade com lista geral da Uniăo Europeia, se aplicável, de todos os tipos de tecidos e células a importar e, se diferente, designaçăo comercial de todos os tipos de tecidos e células a importar;
c) Nome do fornecedor do país terceiro para cada tipo de tecidos e células a importar.
4 - Descriçăo das atividades:
a) Lista especificando as atividades de dádiva, colheita, análise, processamento, preservaçăo ou armazenamento efetuadas antes da importaçăo pelo fornecedor do país terceiro, por tipo de tecidos ou células;
b) Lista especificando as atividades de dádiva, colheita, análise, processamento, preservaçăo ou armazenamento efetuadas antes da importaçăo por subcontratados do fornecedor de um país terceiro, por tipo de tecidos ou células;
c) Lista de todas as atividades executadas pelo banco de tecidos e células importador após a importaçăo, por tipo de tecidos ou células;
d) Nomes dos países terceiros em que săo executadas as atividades anteriores ŕ importaçăo, por tipo de tecidos ou células.
5 - Dados dos fornecedores de um país terceiro:
a) Nome do(s) fornecedor(es) de um país terceiro;
b) Nome da pessoa de contacto;
c) Endereço para visitantes e, se for diferente, endereço postal;
d) Número de telefone, incluindo o indicativo internacional e, se for diferente, o número de emergęncia;
e) Endereço de correio eletrónico.
6 - Documentaçăo a fornecer com o requerimento:
a) Cópia do contrato celebrado com o(s) fornecedor(es) de um país terceiro.
b) Descriçăo pormenorizada do fluxo de tecidos e células importados, da sua colheita ŕ receçăo no banco de tecidos e células importador.
c) Cópia do certificado de autorizaçăo de exportaçăo do fornecedor de um país terceiro ou, quando năo seja emitida uma autorizaçăo de exportaçăo específica, certificaçăo da autoridade competente do país terceiro autorizando as atividades no setor dos tecidos e células, incluindo exportaçőes, caso em que a documentaçăo deve também incluir os contactos da autoridade competente do país terceiro;
d) Nos países terceiros em que a documentaçăo referida na alínea anterior năo esteja disponível, deve ser fornecida documentaçăo alternativa, nomeadamente relatórios de auditorias ao fornecedor de um país terceiro. |
| |
|
|
|
|
(a que se refere o n.ş 1 do artigo 9.ş)
Requisitos mínimos relativos ŕ documentaçăo a disponibilizar pelos bancos de tecidos e células que pretendam importar tecidos e células de um país terceiro
O banco de tecidos e células requerente deve apresentar a versăo mais atualizada dos seguintes documentos:
1 - Documentaçăo relativa ao banco de tecidos e células que pretenda realizar atividade de importaçăo:
a) Descriçăo das funçőes da pessoa responsável e informaçăo detalhada sobre as suas qualificaçőes e formaçăo relevantes, como estabelecido na Lei n.ş 12/2009, de 26 de março, na sua atual redaçăo;
b) Cópia do rótulo da embalagem primária, do rótulo da embalagem exterior, e fotografia ou descriçăo da embalagem exterior e do contentor de transporte;
c) Lista das versőes relevantes e atualizadas dos procedimentos operacionais normalizados (PON) relativos ŕs atividades de importaçăo, incluindo em matéria de aplicaçăo do Código Único Europeu, de receçăo e armazenagem de tecidos e células importados, de gestăo de reaçőes e incidentes adversos, de gestăo de retiradas de produtos e de rastreabilidade do dador até ao recetor.
2 - Documentaçăo relativa ao fornecedor de um país terceiro:
a) Descriçăo pormenorizada dos critérios utilizados para identificar e avaliar o dador, informaçăo prestada ao dador ou familiares do dador, forma como foi obtido o consentimento do dador ou seus familiares e confirmaçăo da natureza da dádiva, nomeadamente, neste último caso, se foi ou năo voluntária e năo remunerada;
b) Informaçăo pormenorizada sobre o centro de análise utilizado pelo fornecedor de um país terceiro e as análises efetuadas por esse centro;
c) Informaçăo pormenorizada sobre os métodos utilizados durante o processamento dos tecidos e células, incluindo dados sobre a validaçăo de processos críticos;
d) Descriçăo pormenorizada das instalaçőes, equipamentos e materiais críticos e critérios utilizados para o controlo da qualidade e o controlo do ambiente para cada atividade realizada pelo fornecedor de um país terceiro;
e) Informaçăo pormenorizada sobre as condiçőes de disponibilizaçăo dos tecidos e células pelo fornecedor de um país terceiro;
f) Pormenores sobre eventuais subcontratados utilizados pelo fornecedor de um país terceiro, incluindo o nome, a localizaçăo e a atividade realizada;
g) Resumo da mais recente inspeçăo ao fornecedor de um país terceiro pela autoridade competente desse país terceiro, incluindo a data da inspeçăo, o tipo de inspeçăo e as principais conclusőes;
h) Resumo da mais recente auditoria ao fornecedor de um país terceiro efetuada pelo, ou em nome do, banco de tecidos e células importador;
i) Qualquer acreditaçăo nacional ou internacional relevante. |
| |
|
|
|
|
|