|
DL n.º 55/2015, de 17 de Abril UTILIZAÇÃO CONFINADA DE MICRORGANISMOS E ORGANISMOS GENETICAMENTE MODIFICADOS(versão actualizada) O diploma ainda não sofreu alterações |
|
| SUMÁRIO Estabelece as medidas para a utilização confinada de microrganismos geneticamente modificados e de organismos geneticamente modificados, tendo em vista a proteção da saúde humana e do ambiente, transpondo a Diretiva n.º 2009/41/CE, do Parlamento Europeu e do Conselho, de 6 de maio de 2009 _____________________ |
|
Artigo 24.º
Regiões autónomas |
1 - O presente decreto-lei aplica-se às regiões autónomas dos Açores e da Madeira, sem prejuízo das adaptações decorrentes da estrutura própria da administração regional autónoma.
2 - Os serviços e organismos das respetivas administrações regionais devem remeter à APA, I. P., a informação necessária ao cumprimento das obrigações constantes do n.º 4.º do artigo 4.º
3 - O produto das taxas e das coimas aplicadas nas regiões autónomas constitui receita própria destas. |
| |
|
|
|
|
Artigo 25.º
Norma transitória |
| O regime previsto no Decreto-Lei n.º 2/2001, de 4 de janeiro, continua a aplicar-se aos procedimentos de notificação que não se encontrem concluídos à data da entrada em vigor do presente decreto-lei. |
| |
|
|
|
|
Artigo 26.º
Norma revogatória |
É revogado o Decreto-Lei n.º 2/2001, de 4 de janeiro.
Visto e aprovado em Conselho de Ministros de 26 de fevereiro de 2015. - Pedro Passos Coelho - Maria Luís Casanova Morgado Dias de Albuquerque - Rui Manuel Parente Chancerelle de Machete - António de Magalhães Pires de Lima -Artur Álvaro Laureano Homem da Trindade - José Diogo Santiago de Albuquerque - Paulo José de Ribeiro Moita de Macedo - Luís Pedro Russo da Mota Soares.
Promulgado em 6 de abril de 2015.
Publique-se.
O Presidente da República, Aníbal Cavaco Silva.
Referendado em 8 de abril de 2015.
O Primeiro-Ministro, Pedro Passos Coelho. |
| |
|
|
|
|
Técnicas ou métodos de modificação genética e tipos de MGM a que se referem as alíneas a) e e) do n.º 2 do artigo 2.º
1 - Técnicas ou métodos de modificação genética que produzam microrganismos ou organismos que não são abrangidos pelo presente decreto-lei, desde que não envolvam a utilização de moléculas de ácido nucleico recombinante nem de microrganismos ou organismos diferentes dos criados através de uma ou mais das técnicas/métodos adiante referidos:
1.1 - Mutagénese;
1.2 - Fusão celular (incluindo a fusão de protoplastos) de quaisquer espécies procarióticas que possam permutar material genético através de processos fisiológicos conhecidos;
1.3 - Fusão celular (incluindo a fusão de protoplastos), de células de quaisquer espécies eucarióticas, em que se inclui a produção de hibridomas e a fusão de células vegetais;
1.4 - Autoclonagem consistindo na remoção de sequências de ácido nucleico de uma célula de um organismo, seguida ou não de reinserção de parte ou da totalidade de tal ácido nucleico (ou de um seu equivalente sintético), eventualmente após tratamento enzimático ou mecânico, em células da mesma espécie ou em células de espécies filogeneticamente afins que possam permutar material genético entre si através de processos fisiológicos naturais e em que o microrganismo resultante não seja suscetível de ser patogénico para o ser humano, animais ou plantas;
A autoclonagem pode incluir a utilização de vetores recombinantes em que se verifique existir uma ampla experiência de utilização segura no microrganismo em questão.
2 - Critérios destinados a determinar a segurança para a saúde humana e para o ambiente dos MGM
O presente anexo descreve, em termos gerais, os critérios que devem ser preenchidos para determinar a segurança para a saúde humana e para o ambiente de alguns tipos de MGM. Podem ser estabelecidas por comitologia notas técnicas explicativas com vista a facilitar a execução do presente anexo.
Os MGM que não respeitem os critérios a seguir enumerados não estão em condições de ser incluídos no n.º 3.
2.1 - Critérios gerais
2.1.1 - Verificação/autenticação da estirpe
A identidade da estirpe deve ser estabelecida com precisão e a modificação conhecida e verificada.
2.1.2 - Dados de segurança documentados e comprovados
Devem ser fornecidas provas documentais da segurança do organismo.
2.1.3 - Estabilidade genética
Sempre que uma eventual instabilidade possa afetar negativamente a segurança, são exigidas provas de estabilidade.
2.2 - Critérios específicos
2.2.1 - Ausência de patogenicidade
O MGM não deve ser suscetível de causar doenças ou danos a um ser humano, planta ou animal saudáveis. Na patogenicidade incluem-se a toxicidade e o potencial alergénico, pelo que o MGM também deve ser:
2.2.1.1 - Ausência de toxicidade.
O MGM não deve produzir um aumento da toxicidade em resultado da modificação genética, nem distinguir-se pelas suas propriedades toxigénicas.
2.2.1.2 - Não alergénico
O MGM não deve produzir um aumento do potencial alergénico acrescido em resultado da modificação genética, nem ser um alergénio reconhecido, dotado, por exemplo, de um potencial alergénico comparável nomeadamente ao dos microrganismos identificados no Decreto-Lei n.º 84/97, de 16 de abril, alterado pela Lei n.º 113/99, de 3 de agosto.
2.2.2 - Ausência de agentes adventícios nocivos
O MGM não deve conter agentes adventícios conhecidos, tais como outros microrganismos, ativos ou latentes, que coexistam no exterior/interior do MGM e que sejam suscetíveis de causar danos à saúde humana e ao ambiente.
2.2.3 - Transferência de material genético
O material genético modificado não deve causar riscos em caso de transferência, nem ser autotransmissível ou transferível com uma frequência superior à de outros genes do microrganismo recetor ou parental.
2.2.4 - Segurança do ambiente em caso de libertações importantes e involuntárias
Os MGM não devem produzir efeitos adversos, imediatos ou retardados, no ambiente, caso ocorra um incidente que envolva uma libertação significativa e involuntária.
3 - Tipos de MGM que cumprem os critérios referidos no n.º 2:
A aprovar por procedimento de regulamentação com controlo, previsto na Decisão do Conselho n.º 1999/468/CE, de 28 de junho de 1999, que fixa as regras de exercício das competências de execução atribuídas à Comissão, com as alterações que lhe foram introduzidas pela Decisão do Conselho n.º 2006/512/CE, de 17 de julho de 2006. |
| |
|
|
|
|
Técnicas, a que se referem as alíneas c) e e) do artigo 3.º
1 - As técnicas de modificação genética são, entre outras, as seguintes:
1.1 - Técnicas de ácidos nucleicos recombinantes que envolvam a formação de novas combinações de material genético através da inserção de moléculas de ácido nucleico, produzidas por qualquer método fora de um organismo, no interior de qualquer vírus, plasmídeo bacteriano ou outro sistema vetorial e a sua incorporação num organismo hospedeiro, onde não existam naturalmente, mas no qual sejam capazes de propagação continuada;
1.2 - Técnicas que envolvam a introdução direta num microrganismo ou organismo de material hereditário preparado fora desse microrganismo ou organismo, incluindo a microinjeção, a macroinjeção e o microencapsulamento;
1.3 - Técnicas de fusão ou hibridização celular em que haja formação de células vivas com novas combinações de material genético hereditário, através da fusão de duas ou mais células por mecanismos que não ocorram naturalmente.
2 - Técnicas não consideradas como dando origem a modificação genética, desde que não envolvam a utilização de moléculas de ácido nucleico recombinante ou MGM ou OGM produzidos através de técnicas/métodos que não os mencionados no anexo I:
2.1 - Fertilização in vitro;
2.2 - Processos naturais, tais como conjugação, transdução, transformação;
2.3 - Indução da poliploidia. |
| |
|
|
|
|
Elementos a considerar para efeitos da avaliação e da classificação a que se referem a subalínea ii) da alínea a) do n.º 3 do artigo 4.º, as alíneas a) e b) do artigo 6.º e o n.º 1 do artigo 7.º
Para se efetuar a avaliação prévia da utilização confinada de MGM ou OGM em função dos eventuais riscos para a saúde humana e para o ambiente, designadamente para efeito da respetiva classificação de acordo com o disposto no artigo 7.º, devem ser considerados os seguintes elementos:
1 - Elementos de avaliação
1.1 - Devem ser considerados como efeitos potencialmente nocivos:
a) Doenças no ser humano, incluindo os efeitos alergénicos ou tóxicos;
b) Doenças em animais ou plantas;
c) Os que resultam da impossibilidade de tratamento de uma doença ou da inexistência de uma profilaxia eficaz;
d) Os que resultam da fixação ou disseminação no ambiente;
e) Os que resultam da transferência natural para outros organismos do material genético inserido.
1.2 - A avaliação efetuada deve basear-se nos seguintes elementos:
a) Identificação dos efeitos potencialmente nocivos, em particular os associados a:
i) Microrganismo ou organismo recetor;
ii) Material genético inserido (proveniente do microrganismo ou organismo dador);
iii) Vetor;
iv) Microrganismo ou organismo dador (enquanto o mesmo for utilizado durante a operação);
v) MGM ou OGM resultante;
b) Características da atividade;
c) Gravidade dos efeitos potencialmente nocivos referidos no n.º 1;
d) Probabilidade de ocorrência dos efeitos referidos no n.º 1.
2 - Processo
2.1 - O processo de avaliação deve identificar as propriedades nocivas do microrganismo ou organismo recetor e, quando adequado, do microrganismo ou organismo dador, bem como das propriedades nocivas associadas ao vetor ou ao material inserido, incluindo qualquer alteração das propriedades atuais do recetor.
2.2 - São considerados adequadamente incluídos na classe 1 definida na alínea a) do n.º 1 do artigo 7.º, os MGM ou OGM com as seguintes características:
a) Ser improvável que o microrganismo ou organismo recetor ou parental cadoença no ser humano, em animais ou em plantas (1);
b) Ser improvável que o MGM ou OGM cadoença no ser humano, em animais ou em plantas (1) e apresente efeitos adversos no ambiente;
c) A natureza do vetor e do elemento inserido não originar um MGM ou OGM com um fenótipo suscetível de causar doença no ser humano, em animais, ou em plantas (1) ou originar efeitos adversos no ambiente.
2.3 - A classificação das operações de utilização confinada, de acordo com o n.º 1 do artigo 7.º, deve basear-se na legislação comunitária pertinente, nomea-damente a Diretiva n.º 2000/54/CE, bem como as normas constantes do Decreto-Lei n.º 84/97, de 16 de abril, alterado pela Lei n.º 113/99, de 3 de agosto, que transpõe para a ordem jurídica interna as Diretivas do Conselho n.os 90/679/CEE, de 26 de novembro, e 93/88/CEE, de 12 de outubro, e a Diretiva n.º 95/30/CE, da Comissão, de 30 de junho, relativas à proteção da segurança e saúde dos trabalhadores contra os riscos resultantes da exposição a agentes biológicos durante o trabalho, diploma que procede à classificação dos microrganismos, enquanto agentes biológicos, em quatro classes de risco com base nos seus efeitos potenciais sobre uma pessoa adulta saudável.
Essas classes de risco podem ser utilizadas como orientação para a classificação das operações de utilização confinada.
Do mesmo modo, os sistemas nacionais e internacionais (e. g. OMS) de classificação representam igualmente informação de base relevante a ter em consideração.
Estes sistemas dizem respeito aos microrganismos naturais, e, como tal, baseiam-se normalmente na capacidade de os microrganismos causarem doenças no ser humano, nos animais ou nas plantas e na gravidade e transmissibilidade das doenças que podem causar.
O utilizador também pode tomar em consideração os sistemas de classificação dos patogénicos vegetais e animais (habitualmente estabelecidos com base nacional).
Os sistemas de classificação acima referidos apenas dão uma indicação provisória da classe de risco da operação e do nível correspondente de medidas de confinamento e controlo.
2.4 - O disposto nos n.os 2.1 a 2.3 deve conduzir à identificação do nível de risco associado às operações de utilização confinada de MGM ou OGM.
2.5 - A seleção e determinação das medidas de confinamento e outras medidas de proteção são efetuadas com base no nível de risco associado ao MGM ou OGM, em conjunto com os seguintes aspetos:
a) Características do ambiente suscetível de exposição que possam ser negativamente afetadas pelos MGM ou OGM usados na atividade de utilização confinada (e. g. existência de biotas conhecidos que possam ser negativamente afetados pelos microrganismos ou organismos utilizados na atividade de utilização confinada);
b) Características da atividade (e. g. escala e natureza);
c) Quaisquer operações não convencionais (e. g. inoculação de MGM em animais; utilização de equipamento suscetível de gerar aerossóis).
A análise do referido nas alíneas a) a c), em relação à atividade em questão, pode aumentar, diminuir ou deixar sem alteração o nível de risco associado ao MGM ou OGM tal como identificado no n.º 2.4.
3 - A análise efetuada pelo utilizador, de acordo com o disposto nos números anteriores, conduz à classificação da atividade numa das classes previstas no artigo 7.º, com a atribuição de níveis de confinamento.
(1) Apenas se aplica a animais e plantas no ambiente suscetível de exposição. |
| |
|
|
|
|
Medidas de confinamento e outras medidas de proteção a que se referem a subalínea iii) da alínea a) do n.º 3 do artigo 4.º, as alíneas c) e j) do artigo 6.º e o n.º 1 do artigo 7.º
1 - Os quadros que integram o presente anexo estabelecem os requisitos mínimos a que devem obedecer as operações de utilização confinada, consoante a sua classificação e respetivo nível de confinamento.
Com vista a assegurar o confinamento, devem ser adotadas boas práticas de trabalho, de formação e de equipamento de confinamento, bem como de conceção de instalações especiais. Para todas as atividades que envolvam MGM ou OGM, devem ser aplicados os princípios das boas práticas de microbiologia, bem como os seguintes princípios de higiene e segurança no local do trabalho:
a) Manter o nível de exposição a quaisquer MGM ou OGM, quer no local de trabalho quer no ambiente envolvente, o mais baixo possível;
b) Adotar medidas de controlo na fonte, as quais devem ser, eventualmente complementadas com o fornecimento de vestuário e equipamento de proteção individual adequado;
c) Testar e assegurar regularmente a manutenção das medidas de controlo e do equipamento;
d) Efetuar, quando necessário, testes para deteção da presença de organismos manipulados viáveis fora da zona primária de confinamento físico;
e) Assegurar a formação adequada de pessoal;
f) Criar, se necessário, comissões ou grupos de trabalho de segurança biológica, sem direito a qualquer remuneração ou abono;
g) Formular e aplicar regras práticas para a segurança do pessoal;
h) Afixar sinais de perigo biológico onde necessário;
i) Prever instalações de limpeza e descontaminação para o pessoal;
j) Manter e atualizar registos adequados;
k) Interditar comer, beber, fumar, aplicar cosméticos ou guardar alimentos para consumo humano na zona de trabalho;
l) Interditar a pipetagem à boca;
m) Elaborar, sempre que necessário, e disponibilizar procedimentos operacionais normalizados por forma a garantir a segurança;
n) Elaborar procedimentos específicos de desinfeção e disponibilizar desinfetantes eficazes para situações de disseminação de MGM ou OGM;
o) Garantir o fornecimento de sistemas seguros de armazenagem de equipamento e material de laboratório contaminado.
2 - Os requisitos mínimos a observar em atividades laboratoriais encontram-se previstos no Quadro I-A.
3 - Os requisitos mínimos a observar em atividades não laboratoriais encontram-se previstos no Quadro II.
4 - O Quadro I-B prevê as medidas de confinamento e outras medidas de proteção aplicáveis a estufas e recintos de crescimento.
5 - O Quadro I-C prevê medidas de confinamento e outras medidas de proteção aplicáveis a atividades em unidades com animais.
6 - Em certos casos, pode ser necessário aplicar uma combinação de medidas do mesmo nível previstas no Quadro I-A e no Quadro II.
7 - Nos quadros referidos nos números anteriores, o termo «opcional» corresponde à possibilidade de aplicação das medidas, caso a caso, de acordo com a avaliação da utilização confinada em função dos eventuais riscos, a que se refere a alínea a) artigo 6.º
8 - Em certos casos, os utilizadores podem mediante prévia obtenção de acordo da autoridade legalmente competente, não aplicar uma especificação prevista para um dado nível de confinamento ou combinar especificações correspondentes a dois níveis diferentes.
QUADRO I-A
Medidas de confinamento e outras medidas de proteção aplicáveis a atividades laboratoriais
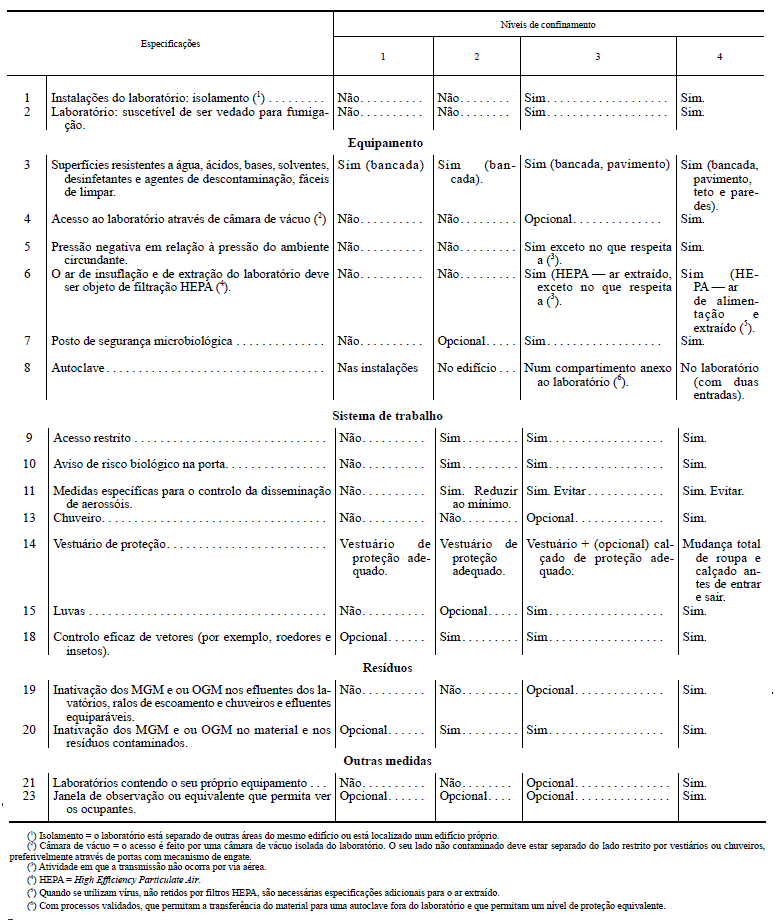
QUADRO I-B
Medidas de confinamento e outras medidas de proteção aplicáveis a estufas e recintos de crescimento
Os termos «estufa» e «recinto de crescimento» referem-se a estruturas com paredes, teto e pavimento, concebidas e utilizadas sobretudo para o crescimento de plantas num ambiente controlado e protegido.
Aplicam-se todas as disposições constantes do Quadro I-A, com os seguintes aditamentos ou alterações:
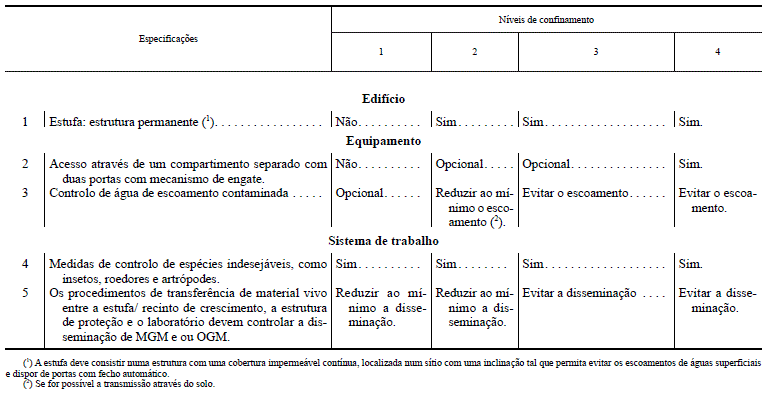
QUADRO I-C
Medidas de confinamento e outras medidas de proteção aplicáveis a atividades em unidades com animais
Aplicam-se todas as disposições constantes do Quadro I-A, com os seguintes aditamentos ou alterações:
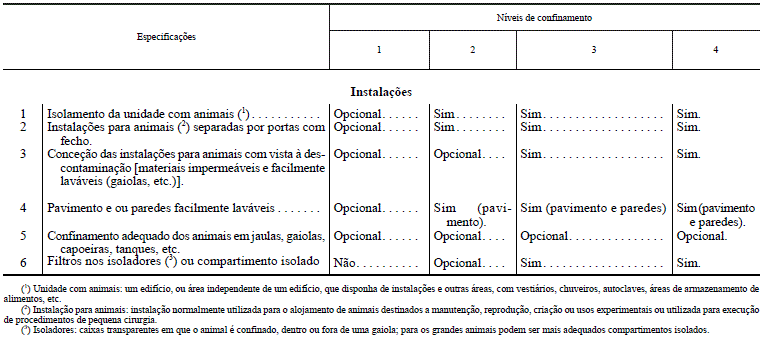
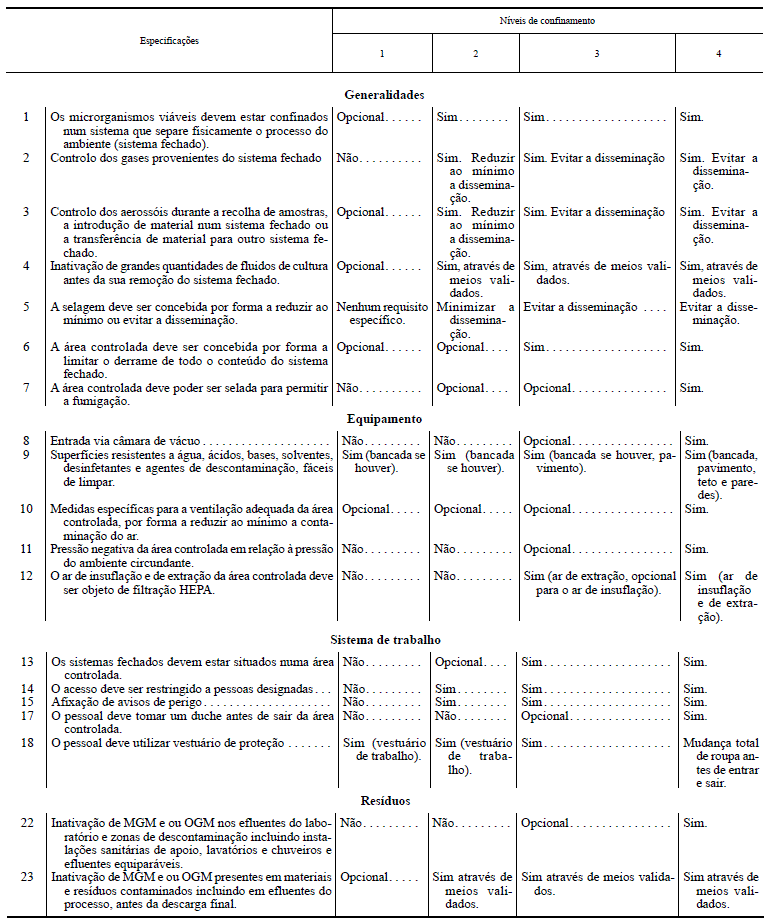
QUADRO II
Medidas de confinamento e outras medidas de proteção aplicáveis nas restantes atividades - Requisitos mínimos
 |
| |
|
|
|
|
Informação a incluir nas notificações a que se referem os n.os 1 e 2 do artigo 8.º, os n.os 1 e 4 do artigo 10.º e o artigo 11.º
1 - Informações necessárias para efeitos da notificação referida no n.º 1 do artigo 8.º:
a) Nome do (s) utilizador (es) e dos responsáveis pela vigilância e segurança;
b) Formação e qualificação dos responsáveis pela fiscalização e segurança;
c) Dados sobre eventuais comissões ou grupos de trabalho biológicos;
d) Endereço da instalação e descrição geral das instalações;
e) Descrição da natureza da atividade a desenvolver;
f) Classe de risco das operações de utilização confinada a efetuar;
g) Resumo da avaliação de risco referida na alínea a) do artigo 6.º e qualquer informação adicional sobre a gestão dos resíduos;
h) Plano de emergência referido na subalínea i) da alínea i) do artigo 6.º
2 - Informações necessárias para a notificação referida na alínea a) do n.º 2 do artigo 8.º e nos n.os 1 e 4 do artigo 10.º:
a) Data da apresentação da notificação referida no artigo 8.º;
b) Nome dos responsáveis pela vigilância e segurança, bem como informação sobre a sua formação e qualificação;
c) Microrganismo(s) ou organismo(s) recetor(es), dador(es) e ou parentais utilizado(s) e, se aplicável, sistema(s) vetor-hospedeiro utilizado(s);
d) Origem (ou origens) e função (ou funções) pretendida(s) do(s) material(is) genético(s) envolvido(s);
e) Identificação e características do(s) MGM ou OGM;
f) Objetivo da utilização confinada, incluindo os resultados previstos;
g) Volumes aproximados de cultura a utilizar;
h) Descrição das medidas de confinamento e outras medidas de proteção a aplicar, incluindo informação sobre a gestão de resíduos, nomeadamente os resíduos a ser gerados, seu tratamento, forma e destino finais;
i) Resumo da avaliação efetuada de acordo com o disposto na alínea a) do artigo 6.º;
j) Dados necessários para que as autoridades competentes possam avaliar os planos de emergência, estabelecidos de acordo com o disposto na subalínea i) da alínea i) do artigo 6.º
3 - Informações necessárias para a notificação referida na alínea b) do n.º 2 do artigo 8.º e no artigo 11.º:
a) Data de apresentação da notificação referida no artigo 8.º;
b) Nomes dos responsáveis pela vigilância e segurança e informações sobre a sua formação e qualificações;
c) Microrganismo(s) ou organismo(s) recetores ou parentais a utilizar;
d) Sistema(s) hospedeiro-vetor a utilizar (se aplicável);
e) Fonte(s) e função (funções) prevista(s) do material genético envolvido na manipulação (ou manipulações);
f) Identificação e características do MGM ou OGM;
g) Volumes de cultura a utilizar;
h) Descrição das medidas de confinamento e outras medidas de proteção a aplicar, incluindo informação sobre a gestão de resíduos, nomeadamente o tipo e características dos resíduos a ser gerados, seu tratamento, forma e destino finais;
i) Objetivo da utilização confinada, incluindo os resultados previstos;
j) Descrição pormenorizada da instalação;
k) Informações relativas à prevenção de acidentes e a planos de emergência, nomeadamente:
i) Riscos específicos decorrentes da localização da instalação;
ii) Medidas preventivas aplicadas, tais como equipamento de segurança, sistemas de alarme e métodos de confinamento;
iii) Procedimentos e planos para verificação da manutenção da eficácia das medidas de confinamento;
iv) Descrição das informações fornecidas ao pessoal;
v) Informação necessária às autoridades competentes para avaliação de quaisquer planos de emergência;
vi) Cópia da avaliação efetuada de acordo com o disposto na alínea a) do artigo 6.º |
| |
|
|
|
|
|