|
Lei n.ş 12/2009, de 26 de Março REGIME JURÍDICO DA QUALIDADE E SEGURANÇA RELATIVA AO TRATAMENTO DE TECIDOS E CÉLULAS ORIGEM HUMANA(versăo actualizada) |
|
|
Contém as seguintes alteraçőes: |
Ver versőes do diploma:
|
|
|
|
|
| SUMÁRIO Estabelece o regime jurídico da qualidade e segurança relativa ŕ dádiva, colheita, análise, processamento, preservaçăo, armazenamento, distribuiçăo e aplicaçăo de tecidos e células de origem humana, transpondo para a ordem jurídica interna as Directivas n.os 2004/23/CE, do Parlamento Europeu e do Conselho, de 31 de Março, 2006/17/CE, da Comissăo, de 8 de Fevereiro, e 2006/86/CE, da Comissăo, de 24 de Outubro _____________________ |
|
ANEXO III
Requisitos para a autorizaçăo de processos de preparaçăo de tecidos e células nos bancos de tecidos e células |
A ASST autoriza cada processo de preparaçăo de tecidos e células após a avaliaçăo dos critérios de selecçăo dos dadores, dos procedimentos de colheita, dos protocolos para cada fase do processo, dos critérios de gestăo de qualidade e dos critérios quantitativos e qualitativos finais para as células e tecidos. Esta avaliaçăo tem de cumprir, pelo menos, os requisitos estabelecidos no presente anexo.
A - Recepçăo nos bancos de tecidos e células
A recepçăo dos tecidos e células deve cumprir os requisitos definidos no artigo 16.ş da presente lei.
B - Processamento
Sempre que as actividades para as quais se solicita autorizaçăo incluírem o processamento de tecidos e células, os procedimentos tęm de cumprir os seguintes critérios:
1 - Os procedimentos críticos de processamento tęm de ser validados e năo podem tornar os tecidos ou células clinicamente ineficazes ou prejudiciais para o receptor. Esta validaçăo pode ser baseada em estudos efectuados pelo próprio serviço ou em dados de estudos publicados ou, para procedimentos de processamento bem estabelecidos, numa avaliaçăo retrospectiva dos resultados clínicos relativos aos tecidos fornecidos pelo serviço.
2 - Tem de ser demonstrado que o processo validado pode ser efectuado de forma consistente e eficaz pelo pessoal no meio ambiente do banco de tecidos e células.
3 - Os procedimentos tęm de ser documentados em PON, que tęm de estar em conformidade com o método validado e com as normas estabelecidas na presente lei, de acordo com o estabelecido em E, n.os 1 a 4, do anexo ii.
4 - Tem de se garantir que todos os processos săo executados em conformidade com os PON aprovados.
5 - Se, nos tecidos ou células, for utilizado um procedimento de inactivaçăo microbiana, tal procedimento deve ser especificado, documentado e validado.
6 - Antes de ser aplicada qualquer alteraçăo significativa ao processamento, o processo alterado tem de ser validado e documentado.
7 - Os procedimentos relativos aos processamentos tęm de ser sujeitos a uma avaliaçăo crítica periódica, incluindo procedimentos, meios ou equipamentos de utilizaçăo em rotina a fim de assegurar que continuam a conduzir aos resultados pretendidos.
8 - Os procedimentos para a eliminaçăo de tecidos e células tęm de evitar a contaminaçăo de outras dádivas e produtos, o meio ambiente de processamento ou o pessoal, em conformidade com a legislaçăo em vigor.
C - Armazenamento e libertaçăo de produtos
Sempre que as actividades para as quais se solicita autorizaçăo incluírem o armazenamento e libertaçăo de tecidos e células, os procedimentos autorizados dos bancos de tecidos e células tęm de cumprir os seguintes critérios:
1 - De acordo com as condiçőes de armazenamento, deve ser especificado o período de armazenamento máximo a fim de garantir as propriedades necessárias.
2 - Tem de existir um sistema de inventário para os tecidos e células para garantir que năo possam ser libertados até terem sido cumpridos todos os requisitos estabelecidos na presente lei.
3 - Tem de existir um procedimento operativo normalizado que defina em pormenor as circunstâncias, responsabilidades e procedimentos para a libertaçăo de tecidos e células para distribuiçăo.
4 - Tem de existir um sistema de identificaçăo de tecidos e células ao longo de qualquer fase do processamento no banco de tecidos e células, o qual tem de permitir uma distinçăo inequívoca entre produtos libertados, em quarentena e eliminados.
5 - Os registos tęm de demonstrar que, antes da libertaçăo dos tecidos e células, săo cumpridas todas as especificaçőes adequadas, nomeadamente que todos os formulários de declaraçăo actuais, registos médicos relevantes, registos de processamento e resultados de análises foram verificados de acordo com um procedimento escrito por uma pessoa autorizada para esta tarefa, pela pessoa responsável referida no artigo 14.ş da presente lei.
6 - Caso se utilize um suporte informático para libertar os resultados do laboratório, o responsável pela respectiva libertaçăo deve poder ser identificado.
7 - Após a introduçăo de qualquer novo critério de selecçăo dos dadores, clínicos ou analíticos, bem como qualquer alteraçăo significativa de uma fase do processamento que melhore a segurança ou a qualidade, tem de ser efectuada uma avaliaçăo do risco documentada, aprovada pela pessoa responsável referida no artigo 14.ş da presente lei, no sentido de determinar o destino de todos os tecidos e células armazenados.
D - Distribuiçăo e retirada
Sempre que as actividades para as quais se solicita autorizaçăo incluírem a distribuiçăo de tecidos e células, os procedimentos autorizados tęm de cumprir os seguintes critérios:
1 - Tęm de ser definidas condiçőes de transporte, tais como a temperatura e o prazo, com vista ŕ conservaçăo das propriedades necessárias dos tecidos e células.
2 - O contentor ou embalagem tęm de ser seguros e garantir que os tecidos e células săo mantidos nas condiçőes especificadas. Todos os contentores e embalagens necessitam de ser validados como adequados ao fim a que se destinam.
3 - Se a distribuiçăo for confiada por contrato a terceiros, tem de existir um acordo documentado que assegure a observância das condiçőes requeridas.
4 - Tem de existir pessoal no banco de tecidos e células autorizado a avaliar a necessidade da retirada de tecidos e células e a desencadear e coordenar as acçőes necessárias.
5 - Tem de existir um procedimento de retirada eficaz que preveja a descriçăo das responsabilidades e das medidas a tomar. Tal procedimento tem de prever a notificaçăo da ASST.
6 - Sempre que um dador possa ter contribuído para causar uma reacçăo no receptor, devem ser tomadas medidas dentro de prazos de tempo preestabelecidos, as quais devem incluir o rastreio dos tecidos e células e, se aplicável, abranger a investigaçăo da origem por forma a identificar os tecidos e células disponíveis provenientes de tal dador e a notificar os destinatários e os receptores dos tecidos e células provenientes desse mesmo dador, caso possam estar em risco.
7 - Tęm de existir procedimentos para o tratamento de pedidos de tecidos e células. As normas para a atribuiçăo de tecidos e células a determinados pacientes ou instituiçőes de cuidados de saúde tęm de ser documentadas e estar disponibilizadas ŕs partes interessadas sempre que solicitado.
8 - Deve existir um sistema documentado para o tratamento de produtos devolvidos, incluindo critérios para a sua aceitaçăo no inventário, se for caso disso.
E - Rotulagem final para distribuiçăo
1 - O rótulo do contentor primário dos tecidos e células deverá indicar:
a) O tipo de tecidos e células, número de identificaçăo ou código dos tecidos ou células, e número do lote ou grupo, se for caso disso;
b) Identificaçăo do banco de tecidos;
c) Prazo de validade;
d) Em caso de dádiva autóloga, este facto tem de ser especificado: «Para utilizaçăo autóloga», e o dador receptor tem de ser identificado;
e) Em caso de dádivas directas, deve ser identificado o receptor;
f) Quando se souber que os tecidos ou células săo positivos para um marcador de uma doença infecciosa relevante, deve ser incluída a mençăo: «Perigo biológico»;
g) O Código Único Europeu aplicável aos tecidos e células distribuídos para aplicaçăo em seres humanos ou a sequęncia de identificaçăo da dádiva aplicável aos tecidos e células colocados em circulaçăo para fins relacionados com processos de preparaçăo prévios ŕ sua distribuiçăo;
h) Caso năo seja possível incluir no rótulo do contentor primário as informaçőes mencionadas nas alíneas d), e) e g), estas devem ser fornecidas em documentaçăo própria, que acompanhará o referido contentor.
2 - Os dados a seguir indicados tęm de constar ou do rótulo, ou da documentaçăo que o acompanha:
a) Descriçăo, definiçăo e, se relevante, as dimensőes do produto ŕ base de tecidos ou células;
b) Morfologia e dados funcionais, se for caso disso;
c) Data de distribuiçăo dos tecidos ou células;
d) Testes biológicos efectuados no dador e respectivos resultados;
e) Recomendaçőes sobre o armazenamento;
f) Instruçőes para a abertura do contentor, embalagem ou qualquer manipulaçăo ou reconstituiçăo necessárias;
g) Prazo de validade após a abertura ou manipulaçăo;
h) Instruçőes para a notificaçăo de reacçőes e incidentes adversos graves, tal como definida no artigo 11.ş da presente lei;
i) Presença de resíduos potencialmente perigosos (antibióticos, óxido de etileno, etc.).
j) No caso de tecidos e células importados, o país de colheita e o país de exportaçăo caso sejam diferentes.
F - Rotulagem exterior do contentor de transporte
Para o transporte, o contentor primário tem de ser colocado num contentor de transporte cujo rótulo contenha, pelo menos, a seguinte informaçăo:
a) Identificaçăo do banco de tecidos e células de origem, incluindo morada e número de telefone;
b) Identificaçăo do organismo de destino responsável pela aplicaçăo em seres humanos, incluindo morada e número de telefone;
c) Uma referęncia de que a embalagem contém tecidos ou células humanas e incluir a mençăo: «Manusear com cuidado»;
d) Sempre que forem necessárias células vivas para funçőes do transplante, tais como células estaminais, gâmetas e embriőes, tem de ser aditada a seguinte expressăo: «Năo irradiar»;
e) Condiçőes de transporte recomendadas (posiçăo, temperatura, etc.);
f) Instruçőes de segurança ou método de refrigeraçăo, sempre que aplicável. |
Contém as alteraçőes dos seguintes diplomas:
- Lei n.ş 99/2017, de 25/08
|
Consultar versőes anteriores deste artigo:
-1Ş versăo: Lei n.ş 12/2009, de 26/03
|
|
|
|
ANEXO IV
Consentimento e informaçőes relativamente ŕ dádiva e aplicaçăo de tecidos e células |
A - Dadores vivos
1 - O consentimento do dador deve ser livre, esclarecido, informado e inequívoco.
2 - O consentimento é prestado perante médico, designado nos termos do disposto no n.ş 2 do artigo 8.ş do anexo ŕ Lei n.ş 22/2007, de 29 de Junho.
3 - Tratando-se de dadores menores, o consentimento deve ser prestado pelos pais, desde que năo inibidos do exercício do poder paternal, ou, em caso de inibiçăo ou falta de ambos, pelo tribunal.
4 - A dádiva de tecidos ou células de menores com capacidade de entendimento e de manifestaçăo de vontade carece também da concordância destes.
5 - A colheita de tecidos ou células em maiores incapazes por razőes de anomalia psíquica só pode ser feita mediante autorizaçăo judicial.
6 - O consentimento do dador ou de quem o represente legalmente é sempre prestado por escrito, sendo livremente revogável, excepto no caso em que, pela preparaçăo pré-transplante já efectuada, a vida do receptor seja posta em risco.
7 - O responsável pelo processo de doaçăo deve assegurar que, no mínimo, o dador ou quem o represente legalmente foi adequadamente informado dos aspectos relativos ŕ doaçăo e ŕ recolha descritos nos n.os 6 e 10 do presente anexo.
8 - A informaçăo tem de ser prestada antes da doaçăo.
9 - A informaçăo deve ser prestada por um profissional de saúde com formaçăo específica nesta área, capaz de a transmitir de forma adequada e clara, usando termos facilmente compreensíveis pelo dador.
10 - A informaçăo deve mencionar a finalidade e a natureza da recolha e as suas consequęncias e riscos, os exames laboratoriais, caso sejam efectuados, o registo e a protecçăo dos dados relativos ao dador, o sigilo médico, o objectivo terapęutico e os benefícios potenciais, bem como informaçăo sobre as salvaguardas aplicáveis destinadas a proteger o dador e o receptor.
11 - O dador, ou quem o representa legalmente, deve ser informado de que tem o direito de receber os resultados confirmados dos testes laboratoriais e de receber explicaçőes claras sobre esses resultados.
12 - Deve ser prestada informaçăo sobre a necessidade da obrigatoriedade de existir o consentimento para que a recolha de tecidos ou células possa efectuar-se.
B - Dadores cadáveres
As informaçőes, os consentimentos e as autorizaçőes devem ser prestados e obtidos de acordo com o previsto na Lei n.ş 22/2007, de 29 de Junho, e no respectivo anexo (republicaçăo da Lei n.ş 12/93, de 22 de Abril - colheita e transplante de órgăos, tecidos e células de origem humana).
C - Dadores de células reprodutivas
As informaçőes, os consentimentos e as autorizaçőes devem ser prestados e obtidos de acordo com o previsto na Lei n.ş 32/2006, de 26 de Julho.
D - Receptor de tecidos e células
1 - A aplicaçăo de tecidos ou células em seres humanos tem de ser precedida do consentimento livre, esclarecido, informado e inequívoco do receptor.
2 - O consentimento é prestado perante médico, designado nos termos do disposto no n.ş 2 do artigo 8.ş do anexo ŕ Lei n.ş 22/2007, de 29 de Junho.
3 - O consentimento é sempre prestado por escrito e livremente revogável.
4 - Tratando-se de receptores menores, o consentimento deve ser prestado pelos pais, desde que năo inibidos do exercício do poder paternal, ou, em caso de inibiçăo ou falta de ambos, pelo tribunal.
5 - A aplicaçăo de tecidos ou células em menores com capacidade de entendimento e de manifestaçăo de vontade carece também da concordância destes.
6 - A aplicaçăo de tecidos ou células em maiores incapazes por razőes de anomalia psíquica só pode ser feita mediante autorizaçăo judicial. |
| |
|
|
|
|
ANEXO V
Critérios de selecçăo de dadores de tecidos e células (excepto dadores de células reprodutivas) |
Os critérios de selecçăo de dadores baseiam-se numa análise dos riscos relacionados com a aplicaçăo dos tecidos ou células específicos. Devem ser identificados indicadores destes riscos por exame físico, uma análise dos antecedentes médicos e comportamentais, análises biológicas, exame post mortem e outras indagaçőes adequadas, no caso de dadores cadáveres. A menos que se justifique com base numa avaliaçăo de riscos documentada, aprovada pela pessoa responsável referida no artigo 14.ş da presente lei, năo devem ser aceites dádivas de dadores aos quais se apliquem os critérios constantes dos números seguintes:
1 - Dadores cadáveres:
1.1 - Critérios gerais de exclusăo:
1.1.1 - Causa de morte indeterminada, a menos que a autópsia revele informaçőes sobre a causa de morte após a colheita e que năo se aplique nenhum dos critérios gerais de exclusăo previstos neste número;
1.1.2 - Antecedentes de doença de etiologia desconhecida;
1.1.3 - Existęncia ou antecedentes de doença maligna, excepto carcinoma basocelular primário, carcinoma do colo do útero in situ e alguns tumores primários do sistema nervoso central, que devem ser avaliados de acordo com dados científicos. Para a dádiva de córnea, podem ser tomados em consideraçăo e avaliados dadores com doenças malignas, excepto retinoblastoma, neoplasias hematológicas e tumores malignos no segmento anterior do olho;
1.1.4 - Risco de transmissăo de doenças causadas por priőes. Este risco aplica-se, nomeadamente, a:
a) Pessoas diagnosticadas com a doença de Creutzfeldt-Jakob, ou com a variante desta doença ou com antecedentes familiares de doença de Creutzfeldt-Jakob năo iatrogénica;
b) Pessoas com antecedentes de demęncia progressiva rápida ou com doenças neurodegenerativas, incluindo as de origem desconhecida;
c) Pessoas tratadas com hormonas derivadas da hipófise humana (por exemplo, hormonas do crescimento) e receptores de transplantes da córnea, esclerótica e dura-máter, bem como pessoas que tenham sido submetidas a intervençăo neurocirúrgica năo documentada (na qual possa ter sido usada dura-máter).
1.1.4.1 - Quanto ŕ variante da doença de Creutzfeldt-Jakob, referida na alínea a) do número anterior, podem ser recomendadas medidas de precauçăo adicionais;
1.1.5 - Infecçăo sistémica năo controlada no momento da dádiva, incluindo infecçőes bacterianas, infecçőes virais, fúngicas ou parasitas sistémicas, ou infecçăo local significativa nos tecidos e células a doar. No tocante ŕs dádivas de olhos, podem ser tomados em consideraçăo e avaliados dadores com septicemia bacteriana, mas apenas quando as córneas forem armazenadas mediante cultura de órgăos, de modo a detectar qualquer contaminaçăo bacteriana do tecido;
1.1.6 - Antecedentes, dados clínicos ou resultados laboratoriais que demonstrem a existęncia de risco de transmissăo de VIH, hepatite B aguda ou crónica, excepto no caso de pessoas com um estatuto de imunidade comprovado, hepatite C e HTLV I/II ou presença de factores de risco destas infecçőes;
1.1.7 - Antecedentes de doença crónica, sistémica e auto-imune, capaz de prejudicar a qualidade do tecido a colher;
1.1.8 - Indicaçőes de que os resultados das análises das amostras de sangue do dador năo săo válidos, devido:
a) Ŕ ocorręncia de hemodiluiçăo, em conformidade com as especificaçőes descritas no n.ş 2 do anexo vi, quando năo estiver disponível uma amostra pré-transfusăo; ou
b) Ao tratamento com agentes imunossupressores;
1.1.9 - Dados de outros factores de risco de doenças transmissíveis, com base numa avaliaçăo dos riscos que tenha em conta os antecedentes do dador em matéria de viagens e exposiçăo, bem como a prevalęncia de doenças infecciosas locais;
1.1.10 - Presença, no corpo do dador, de sinais físicos que sugiram risco de doenças transmissíveis;
1.1.11 - Ingestăo de substâncias ou exposiçăo a substâncias, tais como organofosforados, cianeto, chumbo, mercúrio ou ouro, que possam ser transmitidas aos recetores em doses suscetíveis de pôr em risco a sua saúde;
1.1.12 - Antecedentes recentes de vacinaçăo com vírus vivos atenuados, quando se considere que há risco de transmissăo;
1.1.13 - Transplantaçăo com xenotransplantes.
1.2 - Critérios suplementares de exclusăo de crianças dadoras mortas:
1.2.1 - Devem ser excluídas de dadoras, até que o risco de transmissăo de infecçăo possa ser definitivamente afastado, todas as crianças cujas măes estejam infectadas pelo VIH ou satisfaçam qualquer dos critérios de exclusăo descritos no n.ş 1.1 do presente anexo.
a) Năo podem ser consideradas dadoras, independentemente dos resultados das análises, as crianças com menos de 18 meses de idade cujas măes estejam infectadas ou apresentem factores de risco de infecçăo por VIH, hepatite B, hepatite C ou HTLV e que tenham sido amamentadas pelas respectivas măes nos 12 meses anteriores.
b) Podem ser aceites como dadoras as crianças cujas măes estejam infectadas ou apresentem factores de risco de infecçăo por VIH, hepatite B, hepatite C ou HTLV e que năo tenham sido amamentadas pelas respectivas măes nos 12 meses anteriores e cujas análises, exames físicos e análise de registos clínicos năo demonstrem infecçăo por VIH, hepatite B, hepatite C ou HTLV.
2 - Dadores vivos:
2.1 - Dador vivo para fins autólogos:
2.1.1 - Se as células ou tecidos removidos se destinarem a ser armazenados ou colocados em cultura, deve aplicar-se o mesmo conjunto mínimo de análises biológicas que se aplica aos dadores vivos para fins alogénicos. O facto de os resultados das análises serem positivos năo é impeditivo de que os tecidos ou células ou qualquer outro produto deles derivado sejam armazenados, processados e reimplantados, desde que existam instalaçőes de armazenamento isoladas e adequadas que garantam a inexistęncia de risco de contaminaçăo cruzada para outros transplantes e ou de contaminaçăo com agentes adventícios e ou trocas de produtos.
2.2 - Dador vivo para fins alogénicos:
2.2.1 - Os dadores vivos para fins alogénicos devem ser seleccionados com base nos seus antecedentes sanitários e médicos, fornecidos num questionário e mediante entrevista realizada ao dador por um profissional de cuidados de saúde qualificado e formado, em conformidade com o disposto no n.ş 2.2.5 do presente anexo;
2.2.2 - A avaliaçăo a que se refere o número anterior deve incluir factores relevantes que possam ajudar a identificar e a excluir pessoas cujas dádivas poderiam apresentar um risco para a saúde de terceiros, como a possibilidade de transmissăo de doenças, ou para a sua própria saúde;
2.2.3 - Qualquer que seja a dádiva, o processo de colheita năo deve interferir nem comprometer a saúde do dador nem os cuidados a prestar-lhe;
2.2.4 - No caso de dádivas do cordăo umbilical ou da membrana amniótica, o disposto nos números anteriores aplica-se tanto ŕ măe como ao bebé;
2.2.5 - Os critérios de selecçăo de dadores vivos para fins alogénicos devem ser estabelecidos e documentados pelo banco de tecidos e células e pelo clínico responsável pelos transplantes, no caso de distribuiçăo directa ao receptor, com base no tecido ou células específicos a doar, juntamente com o estado físico do dador, os antecedentes médicos e comportamentais, os resultados de investigaçőes clínicas e de análises laboratoriais que determinem o estado de saúde do dador;
2.2.6 - Os critérios de exclusăo a aplicar devem ser os mesmos que os utilizados no caso de dadores mortos, com excepçăo do disposto no n.ş 1.1.1 do presente anexo. Em funçăo do tecido ou célula a doar, podem ser necessários outros critérios de exclusăo específicos, tais como:
a) Gravidez, excepto para dadores de células do sangue do cordăo umbilical, da membrana amniótica e de irmăos dadores de células progenitoras hematopoiéticas;
b) Amamentaçăo;
c) No caso de células progenitoras hematopoiéticas, as potencialidades de transmissăo de afecçőes herdadas. |
Contém as alteraçőes dos seguintes diplomas:
- Lei n.ş 99/2017, de 25/08
|
Consultar versőes anteriores deste artigo:
-1Ş versăo: Lei n.ş 12/2009, de 26/03
|
|
|
|
ANEXO VI
Análises laboratoriais exigidas a dadores (excepto dadores de células reprodutivas) |
1 - Análises biológicas exigidas aos dadores:
1.1 - Constitui um requisito mínimo submeter todos os dadores ŕs análises biológicas a seguir indicadas:
a) VIH 1 e 2 (anti-VIH-1,2);
b) Hepatite B (HBsAg; anti-HBc);
c) Hepatite C (anti-HCV-Ab);
d) Sífilis, nos termos do n.ş 1.4 do presente anexo.
1.1.1 - Para a hepatite B, hepatite C e HIV devem realizar-se sempre testes aos ácidos nucleicos. Em situaçőes de urgęncia, estes testes podem ser realizados a posteriori.
1.2 - As análises de anticorpos de HTLV I/II devem realizar-se no caso de dadores que vivam ou sejam provenientes de zonas com elevada prevalęncia, ou com parceiros sexuais provenientes dessas zonas, ou no caso de os pais do dador serem provenientes dessas zonas;
1.3 - Quando a análise anti-HBc for positiva e a HBsAg for negativa, dever-se-ăo prosseguir as investigaçőes, mediante avaliaçăo dos riscos, a fim de se determinar a elegibilidade para utilizaçăo clínica.
1.4 - Deve aplicar-se um algoritmo de análise validado a fim de excluir a presença de infecçăo activa com Treponema pallidum. Uma análise năo reactiva, específica ou năo, pode permitir a aceitaçăo de tecidos e células. Quando se realizar uma análise năo específica, um resultado reactivo năo impede a colheita ou a aceitaçăo, caso uma análise específica para confirmaçăo de Treponema seja năo reactiva. Se uma amostra do dador for reactiva a uma análise específica para detecçăo de Treponema, será necessária uma avaliaçăo exaustiva dos riscos a fim de determinar a elegibilidade para utilizaçăo clínica.
1.5 - Em determinadas circunstâncias, podem ser necessárias análises adicionais, em funçăo dos antecedentes do dador e das características do tecido ou células doados, tais como RhD, HLA, malária, CMV, toxoplasma, EBV, Trypanosoma cruzi.
1.6 - Em relaçăo aos dadores para fins autólogos, é aplicável o disposto no n.ş 2.1 do anexo v.
2 - Requisitos gerais a observar na determinaçăo dos marcadores biológicos:
2.1 - As análises devem ser efectuadas por um laboratório aprovado como centro de análise pela autoridade responsável, recorrendo, se necessário, a kits de ensaio com a marcaçăo CE. O tipo de análise utilizado deve ser validado para o efeito, em conformidade com os actuais conhecimentos científicos;
2.2 - As análises biológicas săo efectuadas no soro ou plasma do dador; năo devem ser realizadas noutros fluidos ou secreçőes, como o humor aquoso ou vítreo, a menos que tal se justifique do ponto de vista clínico, devendo utilizar-se uma análise validada para esse fluido;
2.3 - Caso os dadores potenciais tenham perdido sangue e recebido recentemente sangue, componentes sanguíneos, colóides ou cristalóides provenientes de dádivas, a análise do sangue pode năo ser válida devido ŕ hemodiluiçăo da amostra. Deve aplicar-se um algoritmo a fim de avaliar o grau de hemodiluiçăo nas circunstâncias seguintes:
a) Amostragem de sangue ante mortem: se se procedeu a infusăo de sangue, componentes sanguíneos e ou colóides nas 48 horas que antecederam a amostragem do sangue ou se se procedeu a infusăo de cristalóides na hora que precedeu a referida colheita;
b) Amostragem de sangue post mortem: se se procedeu a infusăo de sangue, componentes sanguíneos e ou colóides nas 48 horas que antecederam a morte ou se se procedeu a infusăo de cristalóides na hora que precedeu a morte;
2.3.1 - Os bancos de tecidos e células só podem aceitar tecidos e células de dadores com diluiçăo de plasma superior a 50 /prct. se os procedimentos de análise utilizados estiverem validados para esse plasma ou se dispuserem de uma amostra pré-transfusăo;
2.4 - No caso de um dador cadáver, as amostras de sangue devem ser obtidas imediatamente antes da morte ou, se năo for possível, a colheita de amostras deve realizar-se o mais rapidamente possível após a morte e nunca depois de decorridas 24 horas;
2.5 - A obtençăo da amostra deve observar:
a) No caso de dadores vivos, excepto, por razőes de ordem prática, os dadores de células estaminais de medula óssea e de células estaminais do sangue periférico para fins alogénicos, as amostras de sangue devem ser obtidas no momento da dádiva, ou, se năo for possível, no período de sete dias posteriores ŕ dádiva (a chamada «amostra de dádiva»);
b) Se os tecidos e células de dadores vivos para fins alogénicos puderem ser armazenados durante períodos longos, é necessário fazer uma repetiçăo da amostra e das análises após um intervalo de 180 dias. Nestas circunstâncias, de repetiçăo de análises, a amostra de dádiva pode ser colhida num período compreendido entre 30 dias antes da dádiva e 7 dias após a dádiva;
c) Se os tecidos e células de dadores vivos para fins alogénicos năo puderem ser armazenados durante períodos longos e, consequentemente, năo for possível fazer uma repetiçăo da colheita da amostra, é aplicável o disposto na alínea a) do presente número;
2.6 - Se, num dador vivo, excepto nos dadores de células estaminais de medula óssea e de células estaminais do sangue periférico, a «amostra de dádiva», tal como definida na alínea a) do número anterior, for ainda analisada para determinaçăo de HIV, HBV e HCV, pela técnica de amplificaçăo de ácidos nucleicos (NAT ou TAA), năo é necessário repetir a análise de nova amostra de sangue. Também năo é necessário realizar novas análises quando o processamento incluir uma fase de inactivaçăo que tenha sido validada para os vírus em causa;
2.7 - No caso de colheita de medula óssea e de células do sangue periférico, as amostras de sangue devem ser colhidas para análise nos 30 dias anteriores ŕ dádiva;
2.8 - No caso de dadores neonatais, as análises biológicas ao dador podem ser efectuadas na măe do dador a fim de evitar procedimentos medicamente desnecessários para o bebé. |
Contém as alteraçőes dos seguintes diplomas:
- Lei n.ş 1/2015, de 08/01
|
Consultar versőes anteriores deste artigo:
-1Ş versăo: Lei n.ş 12/2009, de 26/03
|
|
|
|
ANEXO VII
Critérios de selecçăo e análises laboratoriais exigidas a dadores de células reprodutivas |
1 - Tratando-se de dádivas entre parceiros para utilizaçăo directa, năo é necessário aplicar os critérios de selecçăo de dadores.
2 - No caso de dádivas entre parceiros para utilizaçăo năo directa, as células reprodutivas que săo processadas ou armazenadas e as células reprodutivas que derem origem ŕ criopreservaçăo de embriőes devem respeitar os seguintes critérios:
2.1 - O clínico responsável pelo dador deve determinar e documentar, com base nos antecedentes médicos e nas indicaçőes terapęuticas do paciente, a justificaçăo para a dádiva e a segurança desta para o receptor e para as crianças que puderem vir a nascer;
2.2 - Devem efectuar-se as análises biológicas a seguir indicadas a fim de avaliar o risco de contaminaçăo cruzada:
a) VIH 1 e 2 (anti-HIV-1, 2);
b) Hepatite B (HBsAg; anti-HBc);
c) Hepatite C (anti-HCV-Ab);
2.3 - Caso năo estejam disponíveis ou sejam positivos os resultados das análises indicadas no n.ş 2.2 ou caso se saiba que o dador constitui fonte de risco de infecçăo, deve ser concebido um sistema de armazenamento separado;
2.4 - Devem realizar-se análises de anticorpos HTLV I/II em dadores que vivam ou sejam provenientes de zonas com elevada prevalęncia ou com parceiros sexuais provenientes dessas zonas ou no caso de os pais do dador serem provenientes dessas zonas;
2.5 - Em determinadas circunstâncias, podem ser necessárias análises adicionais, em funçăo dos antecedentes do dador relativamente a viagens e eventual exposiçăo a agentes infecciosos e das características do tecido ou células doadas, tais como RhD, malária, CMV, T. Cruzi;
2.6 - O facto de os resultados serem positivos năo é necessariamente impeditivo de dádiva entre parceiros, de harmonia com as legis artis legalmente definidas.
3 - No caso de dádivas năo provenientes de parceiros, a utilizaçăo de células reprodutivas deve respeitar os seguintes critérios:
3.1 - Os dadores devem ser seleccionados com base na idade, saúde e antecedentes médicos, fornecidos num questionário e mediante entrevista pessoal realizada por médico com experięncia. Esta avaliaçăo deve incluir factores relevantes que contribuam para identificar e excluir pessoas cujas dádivas possam apresentar um risco para a saúde de terceiros, como a possibilidade de transmissăo de doenças, tais como infecçőes sexualmente transmitidas, ou para a sua própria saúde, tais como hiperovulaçăo, sedaçăo ou os riscos associados ao procedimento de colheita de óvulos ou ŕs consequęncias psicológicas de se ser dador;
3.2 - Os dadores devem ser negativos para o HIV-1 e 2, a HCV, HBV e sífilis numa amostra de soro ou plasma, analisada em conformidade com o n.ş 1.1 do anexo ii, e os dadores de esperma devem ainda ter negatividade para a Chlamydia numa amostra de urina analisada pela técnica de amplificaçăo de ácidos nucleicos (NAT);
3.3 - Devem realizar-se análises de anticorpos de HTLV I/II em dadores que vivam ou sejam provenientes de zonas com elevada prevalęncia ou com parceiros sexuais provenientes dessas zonas ou no caso de os pais do dador serem provenientes dessas zonas;
3.4 - Em determinadas circunstâncias, podem ser necessárias análises adicionais, em funçăo dos antecedentes do dador e das características do tecido ou células doadas, tais como RhD, malária, CMV, T. Cruzi;
3.5 - Em relaçăo aos dadores para fins autólogos, é aplicável o disposto no n.ş 2.1 do anexo v;
3.6 - Deve proceder-se ao rastreio genético para determinaçăo de genes recessivos autossómicos, que, de acordo com dados científicos internacionais, săo prevalecentes nos antecedentes da etnia do dador, e a uma avaliaçăo do risco de transmissăo de doenças hereditárias, que se sabe estarem presentes na família, após a obtençăo do consentimento. Devem ser prestadas informaçőes completas sobre os riscos associados e sobre as medidas tomadas para a sua atenuaçăo, as quais devem ser comunicadas e claramente explicadas ao receptor.
4 - Requisitos gerais a observar na determinaçăo dos marcadores biológicos:
4.1 - As análises devem ser efectuadas em conformidade com o disposto nos n.os 2.1 e 2.2 do anexo vi;
4.2 - Para dádivas entre năo parceiros, devem ser obtidas amostras de sangue no momento de cada dádiva. Para dádivas entre parceiros (năo para utilizaçăo direta), devem ser obtidas amostras de sangue no prazo de tręs meses antes da primeira dádiva. Para outras dádivas entre parceiros pelo mesmo dador, devem obter-se novas amostras de sangue de acordo com a legislaçăo nacional, mas num prazo năo superior a 24 meses, a contar da obtençăo da amostra anterior.
4.3 - As dádivas de esperma năo provenientes de parceiros devem ficar em quarentena, no mínimo, durante 180 dias. Após o decurso deste período, devem ser repetidas as análises com nova amostra de sangue.
4.3.1 - Se, num dador, a amostra de dádiva de sangue for analisada também para determinaçăo de HIV, HBV e HCV, pela técnica de amplificaçăo de ácidos nucleicos (NAT), năo é necessário testar uma nova amostra de sangue.
4.3.2 - Năo é necessário realizar novas análises quando o processamento incluir uma fase de inactivaçăo que tenha sido validada para os vírus em causa. |
Contém as alteraçőes dos seguintes diplomas:
- Lei n.ş 1/2015, de 08/01
|
Consultar versőes anteriores deste artigo:
-1Ş versăo: Lei n.ş 12/2009, de 26/03
|
|
|
|
ANEXO VIII
Procedimentos de dádiva e colheita de células e tecidos e recepçăo no banco de tecidos e células |
1 - Procedimentos de dádiva e colheita:
1.1 - Consentimento e identificaçăo do dador:
1.1.1 - Antes de se prosseguir com a colheita de tecidos e células, uma pessoa autorizada deve confirmar e registar:
a) Que o consentimento para a colheita foi obtido em conformidade com o disposto no artigo 24.ş da presente lei; e
b) De que forma e por quem o dador foi correctamente avaliado.
1.1.2 - No caso de dadores vivos, o profissional de saúde responsável pela obtençăo dos antecedentes de saúde deve assegurar que o dador:
a) Compreendeu a informaçăo prestada;
b) Teve oportunidade de fazer perguntas e que obteve respostas satisfatórias;
c) Confirmou que, tanto quanto lhe é dado saber, todas as informaçőes que prestou săo verdadeiras.
1.2 - Avaliaçăo do dador:
1.2.1 - Uma pessoa autorizada deve recolher e registar as informaçőes médicas e comportamentais relevantes do dador, de acordo com os requisitos descritos no n.ş 1.4 do presente anexo.
1.2.2 - A fim de obter as informaçőes adequadas, devem utilizar-se diferentes fontes relevantes, incluindo, pelo menos, uma entrevista com o dador, no caso de dadores vivos, e, quando adequado, o seguinte:
a) Os registos médicos do dador;
b) Uma entrevista com uma pessoa que conhecia bem o dador, no caso de dadores cadáveres;
c) Uma entrevista com o médico assistente;
d) Uma entrevista com o médico de clínica geral;
e) O relatório de autópsia.
1.2.3 - No caso de um dador cadáver e, quando tal se justifique, no caso de um dador vivo, deve também fazer-se um exame físico do corpo a fim de detectar quaisquer sinais que possam bastar para excluir o dador ou devam ser avaliados no contexto dos antecedentes médicos e pessoais do dador.
1.2.4 - Todos os registos do dador devem ser analisados e avaliados para determinar da sua adequaçăo e assinados por um profissional de saúde qualificado.
1.2.5 - O disposto nos n.os 1.2 a 1.2.4 do presente anexo năo é aplicável a dádivas entre parceiros de células reprodutivas nem a dadores para fins autólogos.
1.3 - Procedimentos de recolha de tecidos e células:
1.3.1 - Devem existir procedimentos de colheita adequados ao tipo de dador e ao tipo de dádiva de tecidos ou células, e que protejam a segurança do dador vivo.
1.3.2 - Os procedimentos de colheita devem conservar as propriedades dos tecidos ou células necessárias para a sua finalidade clínica e simultaneamente reduzir ao mínimo a contaminaçăo microbiológica no decurso deste processo, em especial quando os tecidos e células năo puderem subsequentemente ser esterilizados.
1.3.3 - No caso de dádivas provenientes de dadores cadáveres, a zona de acesso deve ser restrita.
1.3.3.1 - Deve usar-se uma zona de trabalho estéril, mediante a utilizaçăo de campos esterilizados.
1.3.3.2 - Os profissionais que procedem ŕ colheita devem estar vestidos de forma adequada para o tipo de colheita.
1.3.3.3 - O pessoal deve lavar e esfregar adequadamente as măos e os braços, usar vestuário e luvas estéreis, viseiras faciais e máscaras de protecçăo.
1.3.4 - No caso de um dador cadáver, o local de colheita deve ser registado e o período que mediou entre a morte e a colheita deve ser especificado a fim de garantir a conservaçăo das propriedades biológicas e físicas necessárias dos tecidos e células.
1.3.5 - Uma vez colhidos os tecidos e as células do corpo de um dador cadáver, o corpo deve ser reconstituído por forma que a sua aparęncia seja tanto quanto possível semelhante ŕ sua forma anatómica original.
1.3.6 - Devem ser registadas e examinadas todas as reacçőes adversas que ocorram durante a colheita e que prejudiquem ou tenham prejudicado um dador vivo, bem como os resultados de investigaçőes destinadas a determinar as causas.
1.3.7 - Devem existir políticas e procedimentos que reduzam ao mínimo o risco de contaminaçăo de tecidos e células por pessoal susceptível de estar infectado com doenças transmissíveis.
1.3.8 - Devem utilizar-se, na colheita de tecidos e células, instrumentos e dispositivos estéreis. Os instrumentos ou os dispositivos devem ser de boa qualidade, validados ou especificamente certificados e sujeitos a manutençăo regular para efeitos de colheita de tecidos e células.
1.3.9 - Para instrumentos reutilizáveis, deve existir um procedimento de limpeza e esterilizaçăo validado para a remoçăo de agentes infecciosos.
1.3.10 - Sempre que possível, devem utilizar-se apenas dispositivos médicos com marca CE e todo o pessoal envolvido deve ter recebido formaçăo adequada sobre a utilizaçăo desses dispositivos.
1.4 - Documentaçăo relativa ao dador:
1.4.1 - Para cada dador deve existir um registo que contenha os seguintes elementos:
a) Identificaçăo do dador: nome próprio, apelido e data de nascimento. No caso de a dádiva envolver măe e filho, o nome e a data de nascimento da măe e o nome, se conhecido, e a data de nascimento do filho;
b) Idade, sexo, antecedentes médicos e comportamentais. A informaçăo recolhida deve ser suficiente para permitir a aplicaçăo dos critérios de exclusăo, se necessário;
c) Resultados do exame do corpo, se aplicável;
d) Fórmula de hemodiluiçăo, se aplicável;
e) Formulário de consentimento ou autorizaçăo, se aplicável;
f) Dados clínicos, resultados das análises laboratoriais e resultados de outras análises realizadas;
g) Caso se realize uma autópsia, os seus resultados devem ser incluídos no registo. Em relaçăo a tecidos e células que năo possam ser armazenados durante períodos prolongados, deve ser gravado um relatório oral preliminar da autópsia;
h) No caso de dadores de células progenitoras hematopoiéticas, a adequaçăo do dador escolhido para o receptor deve ser documentada. Tratando-se de dádivas sem relaçăo de parentesco, quando a organizaçăo responsável pela colheita tiver acesso limitado aos dados do receptor, devem ser facultados ao organismo que procede ŕ transplantaçăo os dados do dador que săo relevantes para confirmar a adequaçăo.
1.4.2 - O organismo que procede ŕ colheita deve criar um relatório de colheita, que é transmitido ao banco de tecidos e células, dele devendo constar, pelo menos, os seguintes elementos:
a) Identificaçăo, nome e endereço do banco de tecidos e células que vai receber as células ou tecidos;
b) Identificaçăo do dador, incluindo a forma como foi identificado e por quem;
c) Descriçăo e identificaçăo dos tecidos e células colhidos, incluindo amostras para análise;
d) Identificaçăo da pessoa responsável pela sessăo de colheita, incluindo assinatura;
e) Data, hora (quando pertinente, início e fim), local da colheita e procedimento (PON) utilizado, incluindo eventuais incidentes ocorridos; quando necessário, condiçőes ambientais da instalaçăo de colheita (descriçăo da área física em que se procedeu ŕ colheita);
f) Em relaçăo a dadores cadáveres, as condiçőes em que o cadáver é mantido: refrigerado (ou năo), hora do início e do termo da refrigeraçăo;
g) Identificaçăo/números de lote de reagentes e soluçőes de transporte utilizadas;
h) Quando possível, a data e a hora da morte.
1.4.2.1 - Quando se colher esperma no domicílio, o relatório de colheita deve registar este facto e conter apenas os seguintes elementos:
a) Nome e endereço do banco de tecidos e células que vai receber as células ou tecidos;
b) Identificaçăo do dador e, se possível, a data e hora da colheita.
1.4.3 - Todos os registos devem ser claros e legíveis, protegidos contra alteraçőes proibidas, conservados e prontamente acessíveis nestas condiçőes durante todo o seu período de conservaçăo especificado, em conformidade com o disposto na Lei da Protecçăo de Dados Pessoais.
1.4.4 - Os registos do dador necessários para garantir uma total rastreabilidade devem ser conservados durante, no mínimo, 30 anos após a utilizaçăo clínica, ou data de validade, num arquivo adequado, aceitável pela ASST.
1.5 - Embalagem:
1.5.1 - Após a colheita, todos os tecidos e células colhidos devem ser embalados de forma a reduzir ao mínimo o risco de contaminaçăo e armazenados a temperaturas que preservem as características necessárias e a funçăo biológica das células ou tecidos. A embalagem deve também impedir a contaminaçăo dos responsáveis pelo acondicionamento e transporte de tecidos e células.
1.5.2 - Os tecidos ou células embalados devem ser enviados num contentor adequado para o transporte de materiais biológicos e que mantenha a segurança e a qualidade dos tecidos ou células nele contidos.
1.5.3 - Todas as amostras de tecido ou sangue para análise que os acompanhem devem estar rotuladas com exactidăo a fim de assegurar a identificaçăo do dador, devendo incluir o registo da hora e do local em que a amostra foi colhida.
1.6 - Rotulagem dos tecidos ou células colhidos:
1.6.1 - No momento da colheita, cada embalagem que contenha tecidos e células deve ser rotulada.
1.6.2 - O contentor primário de tecidos ou células deve indicar a identificaçăo ou o código da dádiva e o tipo de tecidos e células.
1.6.3 - Quando a dimensăo da embalagem o permitir, devem ser fornecidas ainda as seguintes informaçőes:
a) Data da dádiva e, se possível, hora;
b) Advertęncias de perigo;
c) Natureza de eventuais aditivos (se utilizados);
d) No caso de dádivas para fins autólogos, o rótulo deve indicar «Apenas para utilizaçăo autóloga»;
e) Em caso de dádivas directas, o rótulo deve identificar o receptor a que se destinam.
1.6.4 - Caso năo seja possível incluir no rótulo da embalagem primária as informaçőes mencionadas nas alíneas a) a e) do número anterior, devem ser fornecidas numa folha separada que acompanha a embalagem primária.
1.7 - Rotulagem do contentor de transporte - se os tecidos ou células forem transportados por um intermediário, os contentores de transporte devem conter nos respectivos rótulos, pelo menos, os seguintes elementos:
a) As mençőes: «Tecidos e células» e «Manusear com cuidado»;
b) Identificaçăo do estabelecimento a partir do qual a embalagem é transportada (endereço e número de telefone) e o nome da pessoa a contactar em caso de problemas;
c) Identificaçăo do banco de tecidos e células de destino (endereço e número de telefone) e pessoa a contactar para a recepçăo do contentor;
d) Data e hora do início do transporte;
e) Especificaçőes relativas ŕs condiçőes de transporte que sejam importantes para a qualidade e a segurança dos tecidos e células;
f) No caso de todos os produtos celulares, deve ser incluída a seguinte mençăo: «Năo irradiar»; e
g) Se se souber que um produto é positivo a um marcador de uma doença infecciosa relevante, deve ser incluída a mençăo: «Perigo biológico»;
h) No caso de dadores para fins autólogos, deve ser incluída a seguinte mençăo: «Apenas para fins autólogos»;
i) Especificaçőes relativas ŕs condiçőes de armazenamento, tais como: «Năo congelar».
2 - Recepçăo dos tecidos ou células no banco de tecidos e células:
2.1 - Quando os tecidos ou células chegam ao banco de tecidos e células, deve proceder-se ŕ verificaçăo e documentar que a remessa, incluindo as condiçőes de transporte, a embalagem, a rotulagem e a documentaçăo e amostras associadas respeitam os requisitos do presente anexo e as especificaçőes do serviço receptor.
2.2 - Cada banco de tecidos e células deve garantir que os tecidos e as células recebidos sejam colocados em quarentena até serem inspeccionados ou verificados, bem como a respectiva documentaçăo, em conformidade com os requisitos. A análise das informaçőes pertinentes respeitantes ao dador e ŕ colheita e, por conseguinte, ŕ aceitaçăo da dádiva deve ser efectuada por pessoas autorizadas.
2.3 - Cada banco de tecidos e células deve dispor de uma política e de especificaçőes documentadas, que servirăo de termo de comparaçăo aquando da verificaçăo de cada remessa de tecidos e células, incluindo amostras. Delas devem constar requisitos técnicos e outros critérios que o banco de tecidos e células considerar essenciais para a manutençăo de uma qualidade aceitável.
2.3.1 - O banco de tecidos e células deve dispor de procedimentos documentados para a gestăo e a separaçăo de remessas năo conformes ou relativamente ŕs quais năo se disponha de resultados de análises completos a fim de assegurar a inexistęncia do risco de contaminar outros tecidos e células que estăo a ser processados, preservados ou armazenados.
2.4 - Os dados que devem ser registados no banco de tecidos e células, excepto no caso de dadores de células reprodutivas destinadas a dádivas entre parceiros, incluem os seguintes elementos:
a) Consentimento ou autorizaçăo, incluindo as possíveis utilizaçőes dos tecidos e células (como fins terapęuticos ou de investigaçăo, ou ambos) e todas as instruçőes específicas para eliminaçăo, caso o tecido ou as células năo sejam utilizados para os fins relativamente aos quais se obteve o consentimento;
b) Todos os registos exigidos em relaçăo ŕ colheita e aos antecedentes do dador, conforme descrito no n.ş 1.4 do presente anexo;
c) Resultados do exame físico, das análises laboratoriais ou outras, tais como o relatório de autópsia, caso tenha sido utilizado em conformidade com o n.ş 1.2.2 do presente anexo;
d) No caso de dadores para fins alogénicos, análise correctamente documentada da avaliaçăo completa do dador, em funçăo dos critérios de selecçăo, por uma pessoa autorizada e formada;
e) No caso de culturas de células destinadas a utilizaçăo para fins autólogos, documentaçăo da eventualidade de o receptor ser alérgico a medicamentos.
2.5 - No caso de células reprodutivas destinadas a dádivas entre parceiros, os dados que devem ser registados no banco de tecidos e células incluem os seguintes elementos:
a) Consentimento ou autorizaçăo, incluindo as possíveis utilizaçőes dos tecidos e células, tais como para fins reprodutivos apenas ou para fins terapęuticos ou de investigaçăo, e todas as instruçőes específicas para eliminaçăo, caso o tecido ou as células năo sejam utilizados para os fins relativamente aos quais se obteve o consentimento;
b) Identificaçăo e características do dador: tipo de dador, idade, sexo e presença de factores de risco;
c) Identificaçăo do parceiro;
d) Local da colheita;
e) Tecidos e células obtidos e características relevantes. |
| |
|
|
|
|
ANEXO IX
Sistema de biovigilância |
|
ANEXO X
Dados mínimos a conservar em conformidade com o artigo 8.ş |
A - Pelas unidades de colheita e bancos de tecidos e células:
Identificaçăo do dador;
Identificaçăo da dádiva que incluirá, pelo menos:
Identificaçăo do organismo de colheita (incluindo os contactos) ou do banco de tecidos e células;
Número único de identificaçăo das dádivas;
Data da colheita;
Local da colheita;
Tipo de dádiva (por exemplo, um tecido ou vários tecidos; autóloga ou alogénica; dadores vivos ou dadores mortos);
Identificaçăo do produto que incluirá, pelo menos:
Identificaçăo do banco de tecidos e células;
Tipo de produto ŕ base de tecidos/células (nomenclatura básica);
Número da pool (se aplicável);
Número do fraccionamento (se aplicável);
Data de validade (se aplicável);
Estatuto dos tecidos ou células (por exemplo, em quarentena, adequadas para utilizaçăo, etc.);
Descriçăo e origem dos produtos, etapas de processamento aplicadas, materiais e aditivos que entraram em contacto com os tecidos e células e que influenciam a sua qualidade e ou segurança;
Código Único Europeu (se aplicável);
Identificaçăo da instalaçăo que emite o rótulo final;
Identificaçăo da aplicaçăo em seres humanos que incluirá, pelo menos:
Data de distribuiçăo ou eliminaçăo;
Identificaçăo do clínico ou utilizador final/instalaçăo.
B - Pelos serviços responsáveis pela aplicaçăo de tecidos e células em seres humanos:
a) Identificaçăo do banco de tecidos e células ou unidades de colheita fornecedoras;
b) Identificaçăo do clínico ou utilizador final/instalaçăo;
c) Tipo de tecidos e células;
d) Identificaçăo do produto;
e) Identificaçăo do receptor;
f) Data da aplicaçăo.
g) Código Único Europeu (se aplicável). |
Contém as alteraçőes dos seguintes diplomas:
- Lei n.ş 99/2017, de 25/08
|
Consultar versőes anteriores deste artigo:
-1Ş versăo: Lei n.ş 12/2009, de 26/03
|
|
|
|
ANEXO XI
Informaçăo contida no Código Único Europeu |
a) Sequęncia de identificaçăo da dádiva:
i) Código do banco de tecidos e células;
ii) Número único da dádiva;
b) Sequęncia de identificaçăo do produto:
i) Código do produto;
ii) Número do fracionamento;
iii) Data de validade.
Estrutura do Código Único Europeu
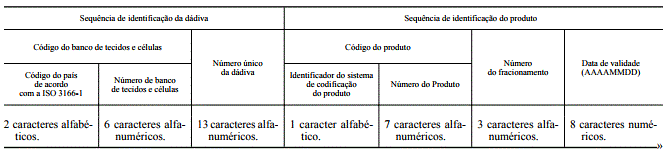 |
Contém as alteraçőes dos seguintes diplomas:
- Lei n.ş 99/2017, de 25/08
|
Consultar versőes anteriores deste artigo:
-1Ş versăo: Lei n.ş 12/2009, de 26/03
|
|
|
|
ANEXO XII
Dados a registar no Compęndio dos Bancos de Tecidos e Células da EU |
A - Informaçăo sobre o banco de tecidos e células:
1 - Nome do banco de tecidos e células;
2 - Código nacional ou internacional do banco de tecidos e células;
3 - Nome da instituiçăo em que banco de tecidos e células está localizado (se aplicável);
4 - Endereço do banco de tecidos e células;
5 - Contactos publicáveis: correio eletrónico funcional, telefone e fax;
B - Informaçăo sobre a autorizaçăo do banco de tecidos e células:
1 - Nome da(s) autoridade(s) competente(s) de autorizaçăo;
2 - Nome da(s) autoridade(s) nacional(ais) competente(s) responsável(eis) pela manutençăo do compęndio dos bancos de tecidos e células da UE;
3 - Nome do titular da autorizaçăo (se aplicável);
4 - Tecidos e células para os quais foi concedida autorizaçăo;
5 - Atividades efetivamente realizadas para as quais foi concedida autorizaçăo;
6 - Estado da autorizaçăo (concedida, suspensa, revogada, no todo ou em parte, cessaçăo voluntária da atividade);
7 - Detalhes sobre eventuais condiçőes e isençőes aditadas ŕ autorizaçăo (se aplicável).
|
| |
|
|
|
|
|